Úvod do odbourávání a syntézy glukózy
Sacharidy, jedna z hlavních živin heterotrofních organismů, se nacházejí v každé buňce našeho těla, kde plní řadu funkcí – zdroj energie pro buňky, zdroj uhlíkových atomů pro syntézu látek, rezervní forma chemické energie (glykogen) či strukturní funkce (proteoglykany).
Glukóza[upravit | editovat zdroj]
Glukóza (Glc) je univerzální energetický substrát – oxidací jednoho gramu glukózy získáme přibližně 17 kJ, tj. 4 kcal. Značný význam má fakt, že naše buňky z ní dovedou získávat energii i za nepřítomnosti O2. To glukózu odlišuje od ostatních živin. Některé buňky, např. erytrocyty či buňky CNS, na glukóze dokonce striktně závisí. Pyruvátdehydrogenázová reakce (PDH) je nevratná, a proto nelze syntetizovat glukózu z mastných kyselin. Nadbytek sacharidů naopak dokáže naše tělo přeměnit skrze acetyl-CoA na mastné kyseliny a následně na triacylglyceroly (TAG).
Glykémie označuje koncentraci glukózy v krvi. Její normální hladina nalačno činí 3,3–5,6 mmol/l, po jídle však může přechodně vystoupit až na 7,0 mmol/l. Za fyziologických okolností se glukóza nevylučuje močí. Pokud glykémie překročí hodnotu 10 mmol/l (tzv. ledvinný prah pro glukózu), objeví se glukóza v definitivní moči – hovoříme pak o glykosurii.
Glukóza se v potravě vyskytuje buď volná, nebo jako součást disacharidů či polysacharidů. Z trávicího traktu se do krve vstřebává pouze volná glukóza.
Zdroje krevní glukózy[upravit | editovat zdroj]
- Sacharidy z potravy (trávení sacharidů v GIT), případně přeměna jiných živin z potravy na glukózu.
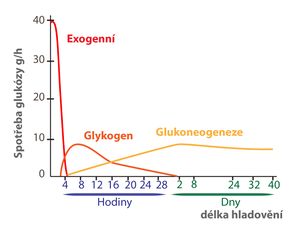
- Rozklad jaterního glykogenu – využívá se mezi jídly. Zásoba jaterního glykogenu vystačí asi na 24 hodin.
- Glukoneogeneze z C3 a C4 látek (laktát, glycerol, většina aminokyselin) je zdrojem glukózy při dlouhodobém lačnění nebo při patologických podmínkách. V době dlouhodobého hladovění činí podíl energie čerpané z glukózy na celkové spotřebě organismu pouze 20 %, větší část energie se získává oxidací lipidů.
Příjemci krevní glukózy[upravit | editovat zdroj]
- Spotřeba tkáněmi závislými na glukóze, jako je mozek, erytrocyty – nezávislé na inzulinu.
- Spotřeba tkáněmi, které nejsou závislé na glukóze, a mohou tedy využívat i jiné energetické substráty, např. kosterní svaly – závislé na inzulinu.
- Syntéza glykogenu v játrech, svalech a dalších tkáních.
- Přebytek glukózy se přemění na mastné kyseliny a TAG – skladování zejména v tukové tkáni.
- Tvorba mnoha významných látek (ostatní monosacharidy, deriváty monosacharidů apod.).
Sacharidy jsou metabolizovány ve formě fosforečných esterů. Klíčová látka v metabolismu sacharidů, glukóza-6-fosfát (Glc-6-P), představuje spojnici mnoha metabolických drah: glykolýzy, glukoneogeneze, pentózového cyklu, glykogeneze a glykogenolýzy. Zároveň udržuje glukózu v buňkách, neboť tento derivát neprochází buněčnou membránou. Fosforylací glukózy je stále udržován koncentrační gradient glukózy mezi extracelulárním a intracelulárním prostorem, což usnadňuje další vstup glukózy do buňky.
Glykolýzu používají vyšší organismy jako hlavní cestu odbourávání sacharidů, pentózový cyklus pak jako cestu doplňkovou.
Mechanismus transportu glukózy přes buněčnou membránu[upravit | editovat zdroj]
Glukóza může být transportována přes membránu dvěma mechanismy:
- usnadněnou difúzí pomocí GLUT přenašečů;
- sekundárně aktivním transportem prostřednictvím SGLT transportérů.
V buněčných membránách se vyskytuje celá řada glukózových transportérů fungujících na principu facilitované difúze. Jedná se o pasivní proces, v jehož průběhu jsou molekuly glukózy převáděny po svém koncentračním gradientu za pomoci přenašeče GLUT 1-7 (GLUcose Transporter). Z nich pouze GLUT 4 závisí na hladině inzulinu. Inzulin po navázání na svůj receptor zvyšuje počet GLUT 4 transportérů v membráně příslušných buněk.
Zde uvádíme základní přehled GLUT transportérů:
- GLUT 1 a 3 – slouží k udržení bazálního vychytávání glukózy tkáněmi, jejichž metabolismus je na glukóze závislý (mozek, erytrocyty, ale také ledviny a placenta).
- GLUT 2 – lokalizovaný na membráně β-buněk pankreatu a hepatocytů, umožňuje také přestup glukózy z resorpčních epitelů (proximální tubulus ledvin, enterocyty střeva) do krve.
- GLUT 4 – je transportérem glukózy v tzv. inzulin-dependentních tkáních – kosterní sval, myokard a tuková tkáň. Jeho vystavení na membráně totiž podmiňuje přítomnost vyšších hladin inzulinu v krvi – přenašeče jsou připraveny ve vezikulech a po vazbě inzulinu na receptor nastává fúze vezikul s buněčnou membránou. K tomu dochází zejména po jídle, kdy zmíněné tkáně zodpovídají za metabolismus až 80 % glukózy z krve. V období mezi jídly ji naopak neresorbují a šetří ji pro tkáně na ní závislé.
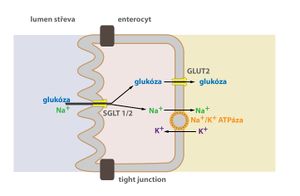
V enterocytech a v buňkách proximálního tubulu ledvin se glukóza vstřebává z lumen aktivním transportem. Přenos glukózy zajišťuje kotransport s Na+. Molekuly glukózy jdou proti svému koncentračnímu gradientu do buňky. Energii poskytnou ionty Na+, které procházejí do buňky po svém koncentračním gradientu. Tento přenos umožňují tzv. SGLT-1 a 2 (Sodium-GLucose Transporter). Ke zpětnému transportu Na+ do ECT se spotřebovává ATP – Na+/K+-ATPáza. Proto hovoříme o sekundárně aktivním transportu.