Endotoxin
Endotoxin je lipopolysacharidový komplex (LPS), který je součástí buněčné stěny gramnegativních bakterií.
Charakteristika[upravit | editovat zdroj]
Pojem endotoxin byl zaveden jako kontrast k exotoxinu, což je toxin uvolňovaný bakteriemi do okolí (endotoxin je uvolněn až po zániku buněčné stěny bakterie). Dnes je pojem endotoxin synonymem pro lipopolysacharid (LPS), který je důležitou součástí vnější membrány gramnegativních bakterií.
Lipopolysacharidy však nejsou pouze škodlivými látkami. Mají důležitou roli i pro bakterii samotnou – přispívají ke strukturní stabilitě a chrání membránu před některými chemickými útoky. Vzhledem k důležitosti lipopolysacharidu pro bakteriální buňku se tato molekula stala terčem výzkumu baktericidních látek.
Složení[upravit | editovat zdroj]
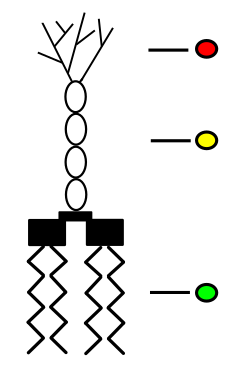
Lipopolysacharid se skládá ze 3 částí:
- lipid A,
- oligosacharidové jádro,
- O-antigen.
Lipid A – tvoří lipidovou složku endotoxinu zodpovědnou za toxicitu gramnegativních bakterií. Díky své hydrofobní povaze (glykolipid) se kotví v jejich vnější membráně. I přes svůj toxický efekt je však rozpoznání lipidu A lidským imunitním systémem klíčové pro zahájení imunitní reakce a její následné zvládnutí. Aktivuje zejména monocyty a makrofágy, k čemuž stačí koncentrace v řádu pikogramů na mililitr krve. Pokud se v lidském těle nachází ve vysokých koncentracích, je možné, že způsobí endotoxický šok, který může skončit smrtí.
Oligosacharidové jádro – je tvořeno krátkým řetězcem sacharidových zbytků (často heptózy, vyskytuje se i ketodeoxyoktulosonová kyselina) a spojuje lipid A s O-antigenem.
O-antigen – tvoří opakující se oligosacharidové jednotky. Nachází se nejzevněji, jedním koncem je připojen k oligosacharidovému jádru a vyčnívá z povrchu mikroba. Je nositelem největší variability a určuje antigenní specifičnost. Pokud má lipopolysacharid kompletní O-řetězec, vypadají kolonie při kultivaci na pevném růstovém médiu jako hladké a vlhké. Jestliže má však O-řetězec zkrácený, pak kolonie vypadají drsně a suše. Takové bakterie mají často zranitelnější membrány hydrofobními antibiotiky. Polysacharidový řetězec je velmi variabilní mezi různými bakteriemi a určuje jejich sérotyp. Cukerné řetězce hladkých lipopolysacharidů mohou překrýt proteiny vnější membrány a zamaskovat je tak před imunitním systémem hostitele.
Uvolnění endotoxinu[upravit | editovat zdroj]
K uvolnění endotoxinu může dojít:
- po fagocytóze a intracelulární destrukci bakterie;
- při rozpadu bakterií účinkem vlastních autolytických enzymů;
- v důsledku cytolýzy komplementem;
- účinkem membránově působících antibiotik.
Biologické účinky[upravit | editovat zdroj]
Působí jako pyrogen (zvýšení teploty). Toxin stimuluje mononukleární fagocyty k produkci endogenních pyrogenů (interleukin-1 a TNF) – vyvolává horečku a vazodilataci. Aktivuje komplementový systém (alternativní dráhou). Důsledkem je cytolýza buňky spojená s dalším uvolňováním toxinu.
Stimuluje odpověď imunitního systému – aktivace makrofágů, neutrofilů, lymfocytů B. Dochází ke vzniku lokální zánětlivé reakce. Při vyšších koncentracích může dojít ke vzniku endotoxického šoku.
Může způsobit poruchy srážlivosti. Aktivuje f. XII – spouští srážecí kaskádu. Ovlivňuje krevní destičky – uvolnění obsahu granul (degranulace trombocytů). Ovlivňuje neutrofily – uvolnění bílkovin stabilizujících fibrinové sraženiny. Ovlivňuje endotelie.
Působí chemotakticky na polymorfonukleáry. Při velkých koncentracích může vzniknout endotoxémie (přítomnost endotoxinu v krvi) – sepse vyvolané G− bakteriemi. Nízká hladina endotoxinu v organismu působí pozitivně (stimulace imunity). Ve velké koncentraci nastává riziko toxického šoku a DIC (často končí smrtí).
- Endotoxický šok
-
- Hypotenze,
- diseminovaná intravaskulární koagulopatie (DIC),
- vazodilatace,
- snížený výkon myokardu (poruchy oxidace).
- 25–40 % těchto případů končí smrtí. Neexistuje efektivní léčba na zvrácení toxické aktivity lipidu A. U infekcí gramnegativními bakteriemi jsou endotoxiny z velké části zodpovědné za závažné klinické projevy. Například u meningokokových infekcí a Waterhouse-Friderichsenova syndromu (selhání nadledvin z důvodu krvácení) způsobených převážně bakterií Neisseria meningitidis.
Endotoxin působí také jako silný mitogen B-lymfocytů a aktivátor polyklonálních B-lymfocytů, což hraje roli v rozvoji odpovídající chronické imunitní odpovědi, pokud nebyla bakterie zničena v akutní fázi.
Kontaminace endotoxiny[upravit | editovat zdroj]
Endotoxiny mohou často kontaminovat látky, se kterými je prováděn výzkum, nebo se jinak medicínsky využívají. To se může týkat například plasmidové DNA pro využití v genové terapii, ovalbuminu ve výzkumu nebo laboratorních pomůcek.
Jedna bakterie Escherichia Coli obsahuje kolem 2 milionů molekul lipopolysacharidu. Endotoxiny jsou navíc velmi tepelně stabilní (nedají se zničit běžnými sterilizačními metodami ani autoklávováním). Díky své hydrofobicitě vykazují velkou afinitu k dalším hydrofobním materiálům, jako jsou například plasty. Pokud by se kontaminace ponechala a došlo by k přenosu do lidského organismu, propukla by zánětlivá reakce, která by mohla být nebezpečná nebo by mohla narušit výsledky testů. Je proto nezbytné endotoxiny odstranit. K tomu se využívá depyrogenace. Tato metoda spočívá v zahřátí až na 250–300 ˚C na 30 minut, což endotoxiny bezpečně zničí.
Velmi citlivá zkouška na přítomnost endotoxinu se nazývá Limulus test, který je založen na principu koagulace krve ostrorepa. Ta se v přítomnosti i malého množství lipopolysacharidu srazí díky velmi silnému amplifikačnímu efektu na enzymy koagulační kaskády.
Možné využití[upravit | editovat zdroj]
Enzymy zapojené v biosyntéze nebo modifikaci lipidu A mohou poskytnout přístup nejen k novým derivátům lipidu A, které mohou být užitečné jako adjuvans nebo antagonisté endotoxinů, ale mohou být využity i pro nové bakteriální vakcíny. Monofosforylovaný lipid A získaný z bakterie Salmonella minnesota se využívá jako adjuvans v kombinaci s kamencem a byl nedávno schválen jako vakcína pro lidský papillomavirus a virovou hepatitidu B.
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
Zdroj[upravit | editovat zdroj]
- JANSKÝ, Petr. Zpracované otázky z mikrobiologie [online]. [cit. 2012-01-30]. <https://www.yammer.com/wikiskripta.eu/uploaded_files/3804405>.
- VOTAVA, Miroslav, et al. Lékařská mikrobiologie obecná. 2. vydání. Brno : Neptun, 2005. ISBN 80-86850-00-5.
- Foca A, Liberto MC, Quirino A, Matera G: Lipopolysaccharides: From Erinyes to Charites, Mediators of Inflammation, Volume 2012 (2012), Article ID 684274, 6 pages
- Lerner KL, Lerner BW: World of Microbiology and Immunology, Gale, Farmington Hills, 2003, s. 351-352