Testosteron
| Testosteron | |
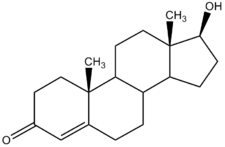 | |
| Prekurzor | cholesterol, progesteron |
|---|---|
| Žláza | endokrinní |
| Účinky | určuje vývoj mužského fenotypu, růst pohlavních orgánů, výskyt sekundárních pohlavních znaků, stimuluje spermatogenezi (u muže) |
| OMIM | 613498 |
Testosteron, nejdůležitější zástupce androgenů, je steroidním hormonem produkovaným u mužů především Leydigovými buňkami. Z jedné třetiny obstarává jeho produkci zona reticularis nadledvin (zde se netvoří přímo testosteron ale jiný androgen s obdobnou funkcí – dehydroepiandrosteron, zkráceně DHEA). Testosteron je odvozen z progesteronu, který vzniká postupnými úpravami uhlíkové kostry cholesterolu (dehydrogenace, izomerace, …).
Morfologie[upravit | editovat zdroj]
Stručná anatomie testes[upravit | editovat zdroj]
Varlata jsou párovým orgánem tvaru elipsoidu o rozměrech v rozmezí 3,6–5,5 cm na délku a 2,1–3,2 cm na šířku. Jejich objem se pohybuje okolo 18,6 ml. Jsou uložena ve scrotu, jež má jednak funkci ochranného obalu a zároveň hraje důležitou roli při regulaci teploty, která by měla být o 3–4 °C nižší než teplota abdominální. Obal varlat je tvořen 3 vrstvami membrán: tunica vaginalis, tunica albuginea a tunica vasculosa. Samotná testes jsou funkčně i morfologicky rozdělena na dva oddíly: intersticium a semenotvorné kanálky. Ty jednotlivě zajišťují dvě hlavní funkce: spermatogenezi a steroidogenezi.
Leydigovy buňky[upravit | editovat zdroj]
Endokrinní elementy varlat, Leydigovy buňky, se nacházejí v intersticiu, které zabírá přibližně 10–15 % varlat a vyplňuje oblast mezi semenotvornými kanálky. Samotné buňky jsou zde zastoupeny 20 % v počtu (asi 350 miliónů). Spolu s Leydigovými buňkami obsahuje intersticium i buňky imunitního systému (makrofágy a lymfocyty), jež svou produkcí cytokinů ovlivňují proliferaci, diferenciaci a endokrinní funkci steroidogenních buněk. Leydigovy buňky jsou původu mesenchymového a vznikly diferenciací fibroblastům podobných buněk intersticia vlivem luteinizačního hormonu. Tyto buňky jsou bohaté na endoplazmatické retikulum a mitochondrie a zároveň v nich můžeme najít hojné lipidové kapénky a lipofuscinová rezidua. Jejich hlavní funkcí je sekrece testosteronu.
Produkce a transport[upravit | editovat zdroj]
Produkci androgenů u muže zajišťují ze 2/3 testes a z 1/3 nadledviny. U ženy jsou naopak nadledviny hlavním zdrojem mužských hormonů, testosteron u nich však zároveň vzniká i v ovariu. Androgeny jsou endokrinně vylučovány přímo do krve, kde jsou transportovány vázané na globulin, konkrétně SHBG. Dále novotvořený testosteron difunduje do Sertoliho buněk, kde se váže na jaderný receptor a na ABP (který zajišťuje transport do lumen) nebo se mění na estradiol, který zpětně difunduje do Leydigových buněk. Androgeny jsou metabolizovány hlavně v játrech a jejich metabolity se vylučují močí.
Regulace sekrece[upravit | editovat zdroj]
Hlavními regulačními mechanismy produkce androgenních hormonů jsou hypotalamo-hypofyzární systém a dále pak lokální autokrinní a parakrinní signalizace. Tyto probíhají cestou:
LH a hCG[upravit | editovat zdroj]
Na vnější membráně Leydigových buněk jsou hojně zastoupeny (až 15 000 na jedné buňce) specifické, vysokoafinitní a nízkokapacitní receptory pro luteinizační hormon.
Při pokusech s laboratorními potkany bylo zjištěno, že koncentrace testosteronu v intersticiu a semenotvorných kanálcích závisí přímo úměrně na čase uplynulém od aplikace LH antisera a v souvislosti s tímto zásahem byl pozorován značný nárůst v počtu místně produkovaných hormonů v intersticiu, které byly stimulovány bazálně ve srovnání s hCG-stimulovanou produkcí testosteronu v izolovaných vyčištěních Leydigových buňkách. [1]
Maximální odpověď se dostavuje už při obsazení 1 % z nich, naopak při přesycení dochází k náhlé redukci jejich počtu. Současně se velká část vazebných schopností ztrácí například při fetálním ozáření varlat, fixaci varlat v abdomen nebo po podvázání chámovodu. LH je jako jediný hormon schopný sám o sobě aktivovat steroidogenezi i v in vitro podmínkách. Zatímco při nízkých dávkách je účinek in vivo maximální, při velkých dávkách může dojít k desenzibilaci buněk na působení hCG i na exogenní cAMP.
Při navázání LH na receptor dochází k stimulaci adenylátcyklázy, která vyvolá v buňce zvýšenou tvorbu cAMP. Tak dochází k aktivaci proteinkinázy, která zajistí biosyntézu specifických proteinů. Na aktivaci proteinkinázy se podílí i druzí poslové: cGMP a Ca2+. Zároveň dochází i k stimulaci aktivity enzymů, které se podílí na štěpení postranního řetězce cholesterolu a jeho uvolnění z esterové vazby. Populace Leydigových buněk je heterogenní a proto nereaguje na stimulaci uniformě. Při nárazovém výskytu vysokých hladin hCG se zablokuje štěpení postranního řetězce cholesterolu, zatímco dlouhodobá mírná stimulace má vliv pozitivní – způsobuje proliferaci organel Leydigových buněk (hlavně hladkého endoplazmatického retikula, mitochondrií a Golgiho komplexu).
Estradiol[upravit | editovat zdroj]
Lokálně produkovaný estradiol může být mediátorem desensibilačních pochodů a jeho hladina citlivě reaguje na stimulaci hCG (už po dvou hodinách je jeho hladina maximální). Estrogeny zároveň inhibují produkci progesteronu.
Adenohypofyzární hormony[upravit | editovat zdroj]
Na rozdíl od Sertoliho buněk nemají buňky Leydigovy receptory pro FSH, zato však nesou receptory pro prolaktin. Ten ale dokáže působit jen synergicky za současné přítomnosti LH. Prolaktin pravděpodobně zvyšuje afinitu LH k receptoru a zároveň ovlivňuje metabolismus lipidů cestou mobilizace esterů cholesterolu a stimulace některých enzymů steroidogeneze. Příliš vysoké hladiny však působí na syntézu testosteronu inhibičně.
Látky produkované přímo varlaty[upravit | editovat zdroj]
Do této skupiny patří například inhibitor vazby LH na receptor, gonadokinin, inhibin… Tyto látky mají z velké části účinky zpomalující až zastavující tvorbu estrogenu.
Další látky a vlivy[upravit | editovat zdroj]
Steroidogeneze je brzděna působením ACTH, glukokortikoidy a stresem, dále je také znám vliv serotoninu a jeho metabolitů na endokrinní funkci varlat.
Mechanismus působení[upravit | editovat zdroj]
Androgenní hormony se stejně jako ostatní tkáňové působky steroidního původu v místě vzniku střádají pouze minimálně, většina produktů steroidogenese je ihned po vytvoření vyloučena do krve. Testosteron (popř. DHEA) pasivně difunduje do buněk cílové tkáně, kde se naváže na androgenní receptor a poté vytvoří komplex hormon-receptor, který vstupuje do jádra, navozuje tvorbu nové mRNA a tím i vznik specifického proteinu.
Biologické účinky testosteronu[upravit | editovat zdroj]
- Testosteron má nepostradatelnou funkci v embryonálním období, kdy určuje vývoj mužského fenotypu (a v posledních dvou měsících embryonální periody iniciuje sestup varlat do scrota).
- Je nezbytný pro růst pohlavních orgánů a výskyt sekundárních pohlavních znaků (ochlupení, mutace), které se nejsilněji projevují během puberty, kdy jeho hladina postupně vzrůstá.
- U muže stimuluje spermatogenezi.
Tato skutečnost byla experimentálně ověřena v roce 1968, kdy byla poprvé prokázána přítomnost androgenů (testosteronu i DHEA) v epididymis králíka. Téhož roku byly tyto steroidy detekovány i v exkretu z caput epididymis berana. V roce 1969 se podařilo popsat syntézu testosteronu in vitro z radioaktivních prekursorů z nadvarlete potkana. (Rozdílnou koncentrací těchto hormonů v jednotlivých oddílech epididymis se zabývá studie A. I. Frankel a K. B. Eik z roku 1970!). [2]
Mimo to ovlivňuje mužské pohlavní chování a svými anabolickými účinky podporuje proteosyntézu. Zároveň zesiluje tvorbu kostí (zvyšuje objem kostní hmoty a ukládání kalcia) a stimuluje růst svalů. Při jeho zvýšené hladině se projevuje negativní vliv na kvalitu kůže (vznik akné). Také zvyšuje erytropoezu cestou zvýšené sekrece erytropoetinu.
Vývojové a funkční poruchy spojené s odchylkami v produkci testosteronu[upravit | editovat zdroj]
- Pseudopubertas je nepravá forma předčasné puberty začínající u chlapců před 9. rokem a u dívek před 8. rokem života. Jednou z příčin jejího vzniku může být autonomní nadprodukce pohlavních hormonů v gonádách nebo nadledvinách. Při léčbě je hlavním cílem zabránit předčasnému ukončení růstu.
- Opožděnou pubertou nazýváme absenci známek pohlavního dospívání u chlapců nad 14 let věku, u dívek od 13 let. Způsobena je naopak sníženou hladinou pohlavních hormonů a léčíme ji jejich substitucí.
- O anorchii hovoříme pokud při nepřítomnosti jednoho nebo obou varlat. Při bilaterální anorchii varlata zanikají až po 16. gestačním týdnu. Postižený má sice maskulizovaný zevní genitál, ale je sterilní a vlivem nízké produkce androgenů se vyznačuje eunuchoidním habitem. Testosteron je nutno doživotně substituovat.
- Kryptorchismus, vyskytující se u 5 % narozených chlapců, přetrvává po 1. roce života u téměř 1/5 z nich. Varlata jsou často dystopická, popř. ektopická co do obvyklé dráhy sestupu. Tvorba testosteronu je zachována, hrozí ale postupné zhoršení spermiogeneze. Zároveň je až třicetkrát zvyšuje riziko maligního zvratu.
- Klinefelterův syndrom vzniká nondisjunkcí XY v meióze. Klasicky se jedná o gonadotyp XXY, vyskytují se ale i případy vícečetných X nebo Y chromozomů. Frekvence výskytu je 1:500 živě narozených chlapců. Typická jsou malá (často azoospermická) varlata, eunuchoidní růst vlivem malé produkce testosteronu a gynekomastie způsobená zvýšenou tvorbou estradiolu. Ochlupení i vousy jsou řidší.
- Syndrom „mužského klimakteria“ (PADAM) je od určitého věku přirozený (viz Obrázek 5) pokles endokrinní aktivity testes zodpovědný za snížení libida, pokles erektility, úbytek svalové hmoty a rozvoj osteoporózy.
- Syndrom necitlivosti na androgeny je podmíněn částečnou nebo úplnou deplecí receptoru pro androgeny. Geneticky bývá lokalizován na lokusu Xp11-12. Při genotypu XY hovoříme o tzv. Morisově syndromu, kdy se vyvíjí fenotyp a psychika ženy, ale se slepě končící vagínou (syndrom testikulární feminizace). Prevalence poruchy je 5/100 000 žen a její léčba spočívá v substituci ženských hormonů a odstranění retinovaných varlat.
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
Externí odkazy[upravit | editovat zdroj]
Zdroj[upravit | editovat zdroj]
Převedeno se svolením autorky Zlatky Vávrové.
Reference[upravit | editovat zdroj]
- ↑ SHARPE, R. M a J. M. S BARTLETT. Intratesticular distribution of testosterone in rats and the relationship to the concentrations of a peptide that stimulates testosterone secretion. Journal of Reproduction and Fertility. 1985, roč. 25, vol. 74, s. 223, ISSN 1741-7899.
- ↑ FRANKEL, A.I a K. B EIK-NES. Testosterone and dehydroepiandrosterone in the epididymis of the rabbit. Journal of Reproduction and Fertility. 1970, roč. 10, vol. 23, s. 441, ISSN 1741-7899.
Použitá literatura[upravit | editovat zdroj]
- STANISLAV, Trojan, et al. Lékařská fyziologie. 4. vydání. Praha : Grada, 2003. ISBN 80-247-0512-5.

