Chromatografie na tenké vrstvě
Chromatografie na tenké vrstvě patří mezi separační metody, oddělující látky ze směsi na základě odlišné afinity jednotlivých složek směsi ke stacionární a mobilní fázi.
U tenkovrstvé chromatografie je skleněná, hliníková nebo plastová deska potažena tenkou vrstvou stacionární fáze (silikagel, oxid hlinitý atd.), na kterou je nanášen analyzovaný vzorek. Látkové množství nanášeného vzorku by nemělo přesáhnout absorpční kapacitu stacionární fáze (je třeba optimalizovat množství vzorku a použitou tloušťku stacionární fáze).
Silikagel[upravit | editovat zdroj]
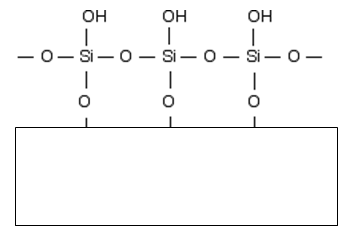
Silikagel je forma oxidu křemičitého, u kterého jsou atomy křemíku mezi sebou navázány přes molekuly kyslíku. Směrem k povrchu destičky jsou na atomy křemíku navázány –OH skupiny. Celá struktura pak vypadá následovně:
Navázané –OH skupiny dávají povrchu destičky polární vlastnosti s možností tvorby vodíkových můstků a dalších nekovalentních interakcí se separovanými látkami.
Mobilní fáze[upravit | editovat zdroj]
Mobilní fáze je specificky definovaná směs rozpouštědel, kterou nalijeme v malé vrstvě (do 1 cm sloupce kapaliny) do chromatografické vany. Poté do vany vložíme chromatografickou desku s naneseným vzorkem tak, aby vzorek byl nad hladinou rozpouštědla a aby se TLC deska opírala o stěnu pouze zadní stranou. Mobilní fáze vzlíná po desce směrem vzhůru a unáší s sebou i analyzovaný vzorek. Rychlost, kterou je vzorek unášen směrem vzhůru, závisí na rozpustnosti vzorku v mobilní fázi a na stupni interakce s fází stacionární (afinitě k stacionární fázi). Čím větší je afinita vzorku ke stacionární fázi, tím pomaleji stoupá vzhůru. Když rozpouštědlo dorazí dostatečně daleko od startu (většinou více než do ¾ desky), vyjmeme desku z chromatografické vany a pozici na desce, kam doputovalo rozpouštědlo, označíme čarou (= čelo).
Retenční faktor[upravit | editovat zdroj]
Poté změříme vzdálenost jednotlivých látek od startu a pro každou látku vypočítáme takzvaný retenční (retardační) faktor Rf. Hodnota Rf udává, jak daleko zaostává skvrna analyzované látky za čelem rozpouštědla. Rf je pro danou látku v daném systému charakteristický, tzn., že pokud experiment zopakujeme, měli bychom ve stejném uspořádání získat stejný Rf. V našem případě bude pro látku A , pro látku B (viz obrázek).
Postup[upravit | editovat zdroj]
V tomto praktickém cvičení budeme používat plastovou destičku potaženou silikagelem. Celý postup by měl probíhat kvůli organické mobilní fázi v digestoři. Na aktivní stacionární fázi nesaháme, při manipulaci s deskou používáme rukavice.
- Nalijeme rozpouštědlo do chromatografické vany, uzavřeme ji víkem a necháme chvíli ekvilibrovat. Výpary rozpouštědla by měly vysytit vnitřní prostor nad hladinou.
- Pipetou nebo stříkačkou naneseme vzorek na TLC desku a nanesenou směs necháme uschnout.
- Odklopíme víko a desku vložíme co nejrychleji dovnitř. Víko ihned zaklopíme.
- Kontrolujeme, aby se čelo rozpouštědla nedostalo až za horní hranu desky. V tom případě by část vzorku "vyjela" ven a nebylo by možné určit Rf.
- Analýzu ukončíme vyjmutím desky z chromatografické vany a označením čela analýzy.
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
Zdroj[upravit | editovat zdroj]
- Leníček M., Muchová L.: Organika I