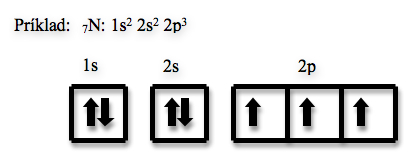
Atom
(přesměrováno z Atóm)
Leukipos a Demokritos – před 2.5 tis. let na základě pozorování přírodních dějů vyslovili teorii, že všechny látky, které existují, jsou složené z malých, nezničitelných a nedělitelných částic – atomů.
Dnešní poznatky: Atomy jsou základní stavební částice chemických látek s poloměrem řádově 10-10m.
Jádro atomu
Atomové jádro se skládá z nukleonů (určených hmotnostním číslem A): protonů (atomové číslo Z) a neutronů (neutronové číslo N). Platí A = Z + N. Číslo Z také udává počet elektronů (atom je elektricky neutrální).
Struktura jádra
Je složené ze dvou mikročástic – protonu a neutronu, které označujeme společným názvem nukleony. Poloměr jádra je přibližně 5·10−15 m.
Proton
Proton je částice, která je nositelem kladného elementárního náboje, má označení p (případně p+, 11p, H+). Počet protonů v jádře atomu je charakteristický pro každý prvek. Počet protonů odpovídá počtu elektronů – elektroneutralita atomu.
Protonové číslo Udává počet protonů v jádře atomu a počet elektronů v obalu elektroneutrálního atomu. Shoduje se s pořadovým číslem prvku v periodické soustavě prvků.
H+ jako proton
Někdy je vodíkový kation, který vznikl disociací kyselin, označovaný též jako proton. Při ztrátě svého jediného elektronu zůstává jen jádro tvořené jedním protonem (u nejlehčího izotopu 11H).
Neutron
Neutron je elektricky neutrální částice rozměrově přibližně stejná s protonem. Počet neutronů v jádře udává neutronové číslo – N' a počet nukleonů v jádře (tzn. protonů + neutronů) udává nukleonové číslo – A.
| Název | Symbol | Pokojová hmotnost [g] |
Náboj [C] | Relativní
elementární náboj |
|---|---|---|---|---|
| proton | p | 1,6726·10−24 | 1,602·10−19 | +1 |
| neutron | n | 1,6750·10−24 | 0 | 0 |
| elektron | e | 9,110·10−28 | −1,602·10−19 | −1 |
Charakteristika jádra
Atomová hmotnost se vyjadřuje v hmotnostních jednotkách: 1 hj = 1,66·10−27 kg. Každý atom je charakterizovaný protonovým a nukleonovým číslem, na základě toho rozlišujeme:
- Izotopy – Složené z atomů, které mají stejné protonové, ale různé nukleonové číslo. Liší se tedy počtem neutronů. Mají stejné chemické vlastnosti, ale odlišují se fyzikálními vlastnostmi. V přírodě se většina prvků vyskytuje v izotopové směsi.
- Izobary – Nuklidy rozličných prvků, které mají stejné nukleonové číslo, ale rozdílné protonové číslo.
- Izotony – Nuklidy rozličných prvků, které mají rozdílné protonové ale taky nukleonové číslo, ale mají stejný počet neutronů v jádře.
- Izomery – Atomy s dočasně zvýšenou celkovou energií, tzn. nestabilní.
Celkový náboj jádra je Z · 1,6·10−19 C. Poloměr jádra vypočítáme podle vzorce: .
Síly v jádře jsou projevem silné jádrové interakce. Působí jen v jádře na vzdálenost cca 10−15 m. Jsou to nejsilnější síly, jaké v přírodě známe.
Radioaktivita
Atomová jádra některých prvků jsou nestabilní a podléhají samovolné přeměně (přírodní radioaktivita), přičemž dochází k emisi záření – ionizující záření.
U přirozených radionuklidů rozeznáváme tyto složky záření:
- záření α- proud atomových jader helia
- záření β- tvořené proudem elektronů;
- záření γ – nejpronikavější, s krátkou vlnovou délkou;
- umělá radioaktivita vzniká například při bombardování jader atomů částicemi α, přičemž vzniká umělý radionuklid.
Elektronový obal atomu
Může obsahovat jeden nebo více elektronů.
Elektron
Mikročástice a nositel záporného náboje s označením e nebo e-. Elektrony v atomu existují jen ve stavech s určitou energií.
Elektrony mohou energii vyzařovat nebo přijímat jen po určitých kvantech, a to při přechodu z jedné energetické hladiny na druhou. Energie kvanta je dána rozdílem energií, které náleží určitým energetickým hladinám v obalu atomu.
Elektron má duální charakter – vlnový a korpuskulární. Tomu odpovídá také princip neurčitosti (není možné určit, kde se elektron nachází a jakou rychlostí se pohybuje). Můžeme jen určit pravděpodobnost − místo s největší pravděpodobností výskytu elektronu se nazývá orbital.
Kvantová čísla
Stav elektronu v obalu atomu popisují 4 kvantová čísla (3 charakterizují orbital a čtvrté projekci spinu konkrétního elektronu v orbitalu).
- Hlavní kvantové číslo (n) – Vyjadřuje energii orbitalu. Nabývá hodnot od 1 do 7 (nebo také označováno jako K, L, M, N, O, P, Q).
- Vedlejší kvantové číslo (l) – Nabývá hodnot od 0 do (n – 1). Udává prostorový tvar a energetickou odlišnost jednotlivých orbitalů.
- Magnetické kvantové číslo (m) – Udává směrovou orientaci orbitalu v magnetickém poli. Nabývá hodnot od -l…0…+l (vedlejší kvantové číslo).
- Spinové kvantové číslo (s) – Nabývá hodnot +1/2 nebo −1/2. V jednom orbitalu můžou být maximálně dva elektrony, které mají opačný spin a vytvářejí elektronový pár.
| Elektr. vrstva | n | l | Typ orbitalu | m | Počet orbitalů | Max. počet elektronů |
|---|---|---|---|---|---|---|
| K | 1 | 0 | 1s | 0 | 1 | 2 |
| L | 2 | 0 1 |
2s 2p |
0 −1, 0, +1 |
1 3 |
8 |
| M | 3 | 0 1 2 |
3s 3p 3d |
0 −1, 0, +1 −2, −1, 0, +1, +2 |
1 3 5 |
18 |
| N | 4 | 0 1 2 3 |
4s 4p 4d 4f |
0 −1, 0, +1 −2, −1, 0, +1, +2 −3, −2, −1, 0, +1, +2, +3 |
1 3 5 7 |
32 |
Pravidla zaplňování orbitalů elektrony
Konfigurace elektronů (iontů)− rozmístění elektronů v jednotlivých orbitalech na jednotlivých vrstvách elektronového obalu. Možné z něj odvodit schopnost atomu (iontu) tvořit určitý typ chemické vazby. Postupné obsazování určuje výstavbový a Pauliho princip a Hundovo pravidlo.
Výstavbový princip – princip minimální energie: Atom v základním stavu má snahu nabývat stavu s nejmenší možnou energií – obsazování orbitalů od těch s nejmenší energií: 1s-2s-2p-3s-3p-4s-3d-4p-5s-4d-5p-6s-4f-5d-6p-7s-5f-6d-7p.
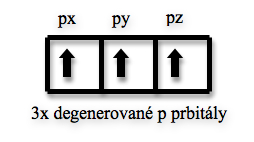
Degenerované orbitaly- mají stejnou energii (mají stejné hlavní a vedlejší kvantové číslo, liší se magnetickým).
Pauliho princip V atomu neexistují dva elektrony, které by měly všechny 4 kvantová čísla stejná (musí se lišit minimálně spinem – znázorníme opačnými šipkami).
Hundovo pravidlo
Degenerované orbitaly se zaplňují tak, aby byl v degenerovaných orbitalech maximální možný počet nespárovaných elektronů (co nejvíc se stejným spinem) a až potom se začnou vytvářet elektronové páry.
Odkazy
Související články
Použitá literatura
- SILNÝ, Peter a Beata BRESTENSKÁ. Prehľad chémie 1. 1. vydání. Bratislava : Slovenské pedagogické nakladateľstvo, 2000. sv. 1. s. 246. ISBN 80-08-00376-6.