Portál:Otázky z biochemie (1. LF UK, VL)/13. Otázka
| 13. Otázka | ||||
| Oxidace a redukce, rovnováha v redoxních reakcích, oxidoredukční potenciál, závislost na koncentraci složek reakce (Nernstova rovnice). Příklady z biochemie. | ||||
| Otázky z biochemie (1. LF UK, VL) | ||||
| Předchozí • Další | ||||
Oxidace a úloha kyslíku
Oxidace je ztráta elektronů, případně zvýšení oxidačního čísla příslušného prvku. Odebrané elektrony musí skončit na jiném prvku, a proto je oxidace jedné látky vždy spojena s redukcí látky jiné. Slovo „oxidace“ pochází ze slova „oxid“, které označuje sloučeninu obsahující kyslík. Kyslík není pro průběh oxidace nezbytně nutný.
Kyslík je oxidační činidlo. Má vysokou tendenci přijímat elektrony. Afinita prvku k elektronům je vyjádřena hodnotou jeho elektronegativity. Elektronegativita kyslíku je jedna z nejvyšších mezi prvky, vyšší má už jenom fluor. Přesun elektronů na kyslík, včetně tvorby vazeb s kyslíkem, je proces termodynamicky výhodný, tzn. uvolňuje energii.
Organizmy žijící na Zemi našly způsob využití energie přenosem elektronů z méně elektronegativních prvků na kyslík. Naše buňky oxidují organické sloučeniny obsažené v potravě na CO2 a H2O za spotřeby kyslíku a produkce energie. Tento proces někdy nazýváme také spalování živin. Na rozdíl od hoření je transfer elektronů z organických molekul na kyslík v našich buňkách rozdělen do mnoha kroků. Většina uvolněné energie se tak nepřemění na teplo a světlo, ale ukládá se ve formě chemického potenciálu. Z didaktických důvodů můžeme oxidativní metabolismus rozdělit do dvou fází:
- Oxidace substrátu spojená s redukcí kofaktorů enzymů;
- Reoxidace redukovaných kofaktorů kyslíkem.
Odbourávání glukózy
Jako příklad můžeme uvést glukózu. Její šestiuhlíkatá molekula (C6H12O6) je v procesu glykolýzy a pyruvátdehydrogenázové reakce postupně oxidována na dvě molekuly kyseliny octové (ve formě acetyl-koenzymu A) a dvě molekuly CO2. Během této reakce dochází k redukci čtyř molekul koenzymu NAD+ (nikotinamidadenindinukleotid) na NADH, přičemž každý přijme dva elektrony (často naznačeno jako přijetí hydridového aniontu H–).
Vytvořený acetyl-CoA vstupuje do citrátového cyklu a je dále oxidován na dvě molekuly CO2 a čtyři molekuly redukovaných kofaktorů (tři NADH a jeden FADH2 – flavinadenindinukleotid). Ve výsledku dochází při oxidaci glukózy k tvorbě 12 redukovaných kofaktorů a šesti molekul CO2. V tomto procesu nedošlo ke spotřebě žádného molekulárního kyslíku (O2) – chybějící atomy kyslíku byly poskytnuty molekulami vody. V té se kyslík vyskytuje již v redukované formě (O–II), která se elektronového transferu neúčastní.
Aby mohla metabolická dráha fungovat, musí být redukované kofaktory zpětně reoxidovány. Proces reoxidace nastává nejčastěji v mitochondriích, kde redukované kofaktory předávají získané elektrony kyslíku (redukují ho). Redukce kyslíku pak vede k uvolnění značného množství energie.
Redoxní potenciál
Oxidačně-redukční potenciál (redoxní potenciál) je měřením schopnosti látek vázat nebo uvolňovat elektrony, tzn. je měřením síly oxidačního nebo redukčního činidla.
Afinitu k elektronům můžeme vyjádřit jako potenciál, na který se nabije elektroda ponořená do roztoku, který obsahuje oxidovanou i redukovanou formu té samé látky – tuto soustavu nazýváme poločlánek.
Jakmile do roztoku, který obsahuje stejné množství redukované a oxidované formy té samé látky, ponoříme elektrodu z ušlechtilého kovu (platinový nebo zlatý drátek), nabije se tato elektroda vhledem k roztoku na určitý potenciál.
- Příklad
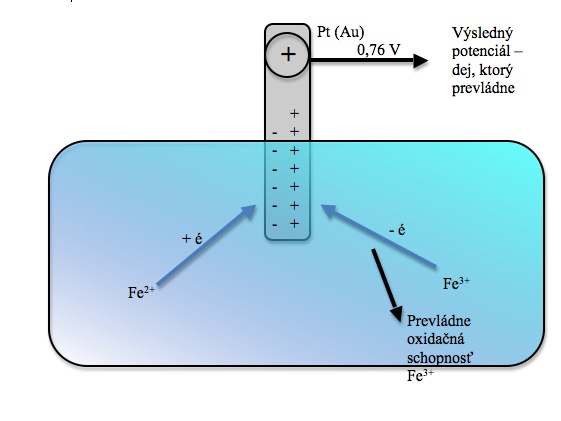
Zaznamenáváme dva protichůdné děje :
- železnaté ionty mají tendenci odevzdávat elektrodě elektrony a vytvářet na ní přebytek záporného náboje, oxidují se na ionty železité,
- železité ionty se snaží elektrodě elektrony odebrat, a tím se redukovat na železnaté, vzniká na ní tak přebytek kladného náboje.
Výsledný potenciál, na který se elektroda nabije, závisí na tom, který z dějů převládne, v našem případě převládne oxidační schopnost železitých iontů a elektroda se nabije kladně na hodnotu 0,76 V (při stejné východní koncentraci obou iontů).
Měření redoxního potenciálu
Nejsme schopni měřit absolutní hodnoty redoxních potenciálů, a tak je porovnáváme s tzv. referenčními elektrodami – mají známý a konstantní potenciál.
- obě elektrody (referenční a i ta, jejíž potenciál chceme změřit) jsou ponořeny v tom samém roztoku a spojené tzv. solným můstkem (nejčastěji roztok KCl) – vytvoří se tím galvanický článek.
Mezinárodní dohoda stanovuje jako základ měření redoxních potenciálů systém vodík, vodíkový kation a platinová elektroda. Redoxní potenciál této skupiny je, podle dohody, nulový a slouží jako základ stupnice redoxních potenciálů.
Nernstova rovnice
Nernstova rovnice slouží k výpočtu elektrochemického rovnovážného potenciálu E libovolného iontu X.
- EX = elektrochemický rovnovážný potenciál iontu X (V)
- R = univerzální plynová konstanta [8,314 472 J/(mol·K)]
- T = absolutní teplota v K (tělesná teplota 37 °C = 310,15 K)
- z = mocenství iontu (např. + 1 pro K+ a Na+, +2 pro Ca2+, −1 pro Cl− apod.)
- F = Faradayova konstanta (96 485,339 9 C/mol)
- ln = přirozený logaritmus
- [X]e = extracelulární koncentrace iontu X
- [X]i = intracelulární koncentrace iontu X
Výše uvedený tvar rovnice lze za určitých podmínek výrazně zjednodušit. Při tělesné teplotě 310 K (tj. 37 °C) je člen RT/F roven číslu 0,0267. Převedeme-li přirozený logaritmus na dekadický (ln x = 2,3 · log10 x), vynásobíme rovnici 1000 (převedení z V na mV), platí
1000 · RT / F · 2,3 · log x = 1000 · 0,0267 · 2,3 · log x = 61 · log x .
Dostáváme tedy
- EX = elektrochemický rovnovážný potenciál iontu X (mV)
- z = mocenství iontu (např. + 1 pro K+ a Na+, +2 pro Ca2+, −1 pro Cl− apod.)
- [X]e = extracelulární koncentrace iontu X
- [X]i = intracelulární koncentrace iontu X
Hodnoty extracelulární a intracelulární koncentrace elektrochemického rovnovážného potenciálu některých iontů jsou uvedeny v následující tabulce:
| Xe (mmol/l) | Xi (mmol/l) | EX (mV) | |
|---|---|---|---|
| Na+ | 145 | 15 | +60 |
| K+ | 4 | 150 | −96 |
| Ca2+ | 2,5 | 10−4 | +134 |
| Cl− | 100 | 5 | −79 |
- [X]e = extracelulární koncentrace iontu X
- [X]i = intracelulární koncentrace iontu X
- EX = elektrochemický rovnovážný potenciál iontu X (mV)
Rovnici formuloval německý chemik Walther Hermann Nernst, který v roce 1920 obdržel Nobelovu cenu za objevy v oblastí fyzikální chemie.





![{\displaystyle E_{X}={\frac {R\cdot T}{z\cdot F}}\cdot \ln {\frac {[\mathrm {X} ]_{e}}{[\mathrm {X} ]_{i}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fe1099f434dabe6cd6b1c1d7fd3cb4d79f1c6876)
![{\displaystyle E_{X}={\frac {61}{z}}\cdot \log {\frac {[\mathrm {X} ]_{e}}{[\mathrm {X} ]_{i}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/75698e8413a765010408d028cafa2469c3329782)