Portál:Otázky z biochemie (1. LF UK, VL, ÚLB)/Základní metody pro separaci makromolekul (elektroforéza, chromatografie, vysolování) a jejich využití v klinické praxi
Elektroforéza
Elektroforéza patří mezi separační metody izolující molekuly o rozdílné hmotnosti, popř. odlišném elektrickém náboji, využívající jejich odlišnou pohyblivost v elektrickém poli.
Z historie
Od roku 1892 je známo, že anorganické částice v koloidním roztoku působením elektrického pole nenáhodně putují. Zanedlouho poté byl tento jev popsán i u proteinů ve vodných roztocích.
V roce 1948 získal za sestavení elektroforetické aparatury NC za chemii švédský vědec Arne W. Tiselius.
Princip elektroforézy
Elektroforéza využívá schopnosti nabitých částic pohybovat se v elektrickém poli, přičemž rychlost pohybu částic je závislá na velikosti celkového povrchového náboje, velikosti a tvaru molekuly a její koncentraci v roztoku.
Rychlost molekuly při elektroforetické separaci lze vyjádřit:
kde ζ je elektrokinetický potenciál (V), ν je lineární rychlost pohybu částice (m ·s−1), E je intenzita elektrického pole (V · m−1) a η viskozita prostředí (Pa · s), εr je relativní permitivita kapaliny, ε0 permitivita vakua, C konstanta závislá na tvaru částic a na tloušťce elektrické dvojvrstvy (např. pro kulovité částice o poloměru r a velkou efektivní tloušťku dvojvrstvy l, kde r/l < 0,1, je C = 2/3, pro tenkou dvojvrstvu (r/l > 100) je C = 1).
Aplikace elektroforézy
Volná elektroforéza
Volná elektroforéza se provádí ve vodných roztocích (elektrolytech), v němž částice putují k elektrodě s opačnou polaritou. Separaci může narušit vliv konvenčních proudů vznikajících vlivem tepla generovaného průchodem elektrického proudu.
Elektroforéza na nosičích
Provádí se na hydrofilních porézních nosičích, jako je např. neklížený papír (chromatografický), acetát celulózy, agarózový gel, polyakrylamidový gel, celulóza, nezgelovatělý škrob apod. Podle materiálu se nosič může chovat jako molekulární síto, jímž procházejí velké molekuly obtížněji než malé.
Zonální elektroforéza plasmatických proteinů
Zonální, také zónová, elektroforéza se provádí např. na acetátcelulóze. Dělení proteinů zde závisí na typu a počtu ionizovatelných skupin postranních řetězců aminokyselin a na velikosti celkového náboje proteinu (kladného nebo záporného).
Je-li pH roztoku, ve kterém elektroforéza probíhá větší, než je pI (izoelektrický bod), protein má celkově záporný náboj. Naopak, je-li pH roztoku nižší, než pI, protein má celkově kladný náboj. Odpovídá-li pH roztoku izoelektrickému bodu proteinu, ten se nepohybuje.
Gelová elektroforéza
Gely tvoří přechod mezi pevným a kapalným stavem. Strukturálně je gel z více než 90 % voda. V gelu nalézáme trojrozměrnou síť, kde póry mohou sloužit jako molekulové síto. Velikost pórů odpovídá velikosti proteinů a nukleových kyselin. Nejčastější gely jsou polyakrylamidový a agarózový.
Agaróza je síť tvořená dlouhými cukernými polymery vázanými nekovalentními vodíkovými můstky a hydrofobními vazbami. Polyakrylamidové gely tvoří síť dlouhých molekul polyakrylamidu spojených příčnými můstky N,N´-metylenbisakrylamidu.
Nativní gelová elektroforéza bílkovin
Probíhá bez denaturačních činidel. Proteiny migrují gelem podle svého celkového náboje, velikosti a tvaru. Citlivost elektroforézy je dána charakterem pórů gelu. Příkladem může být elektroforéza sérových bílkovin.
SDS gelová elektroforéza
Proteiny jsou denaturovány dodecylsíranem sodným (SDS) a β-merkaptoetanolem, který zruší disulfidické vazby. SDS je denaturační činidlo a detergent, který proteiny obalí a denaturuje. Proteiny získají tyčinkovitý tvar a při pH 7–10 mají díky SDS všechny stejnou hustotu povrchového náboje. Jejich pohyblivost závisí téměř výhradně na molekulové hmotnosti polypeptidových řetězců. Metoda je vhodná pro analýzu makromolekulárních komplexů.
Izoelektrická fokusace
Proteiny se dělí v gelu s pH gradientem. Migrují do bodu, kde nemají žádný povrchový náboj, tj. do místa, kde se pH rovná pI.
Dvojrozměrná elektroforéza proteinů
2D elektroforéza umožňuje rozlišení až 10 000 proteinů. Proteiny se nejprve rozdělí podle svých izoelektrických bodů v gradientu pH. Po separaci v prvním rozměru je provedena SDS-elektroforéza v druhém směru, bílkoviny se rozdělí podle své velikosti.
Na rozdíl od předešlých metod, jejichž výsledkem jsou frakce obsahující často směs několika bílkovin, 2D elektroforéza umožňuje izolovat jednotlivé proteiny i z biologických vzorků. Výsledné mapy proteinů se mohou porovnávat s kontrolními vzorky (např. pacienti s konkrétním onemocněním a zdraví pacienti). 2D elektroforéza se používá i jako preparativní metoda: konkrétní skvrna se z gelu vystřihne, izoluje se z ní bílkovina a použije se k další analýze či jinému postupu.
Kapilární elektroforéza
Metoda využívá pohybu elektricky nabitých látek v elektrickém proudu rozpuštěných ve vodivém médiu – kapiláře naplněné elektrolytem nebo gelem. Doprovodným jevem je elektroosmotický tok. Na vnitřním povrchu kapiláry v místě styku s vodivým roztokem vzniká elektrická dvojvrstva. Pevná část (stěna kapiláry) je nabitá nepohyblivým plošným záporným elektrickým nábojem. Z kapalné části se kladné ionty připojí ke stěně kapiláry (dvojvrstva) a ionty se pohybují ke katodě. Pohyblivá vrstvička se žene kapilárou a strhne s sebou celý průřez kapaliny v kapiláře. Roztok putuje kapilárou celý najednou (u elektroforézy putují jen ionty).
Použití elektroforézy
Elektroforéza nalézá široké využití, například při analýze a dělení směsí bílkovin, charakterizace povrchů organizmů jako jsou bakterie, viry apod. Praktické využití při diagnostice postižení monogenních chorob atd.
Chromatografie
Chromatografie na tenké vrstvě patří mezi separační metody, oddělující látky ze směsi na základě odlišné afinity jednotlivých složek směsi ke stacionární a mobilní fázi.
U tenkovrstvé chromatografie je skleněná, hliníková nebo plastová deska potažena tenkou vrstvou stacionární fáze (silikagel, oxid hlinitý atd.), na kterou je nanášen analyzovaný vzorek. Látkové množství nanášeného vzorku by nemělo přesáhnout absorpční kapacitu stacionární fáze (je třeba optimalizovat množství vzorku a použitou tloušťku stacionární fáze).
Silikagel
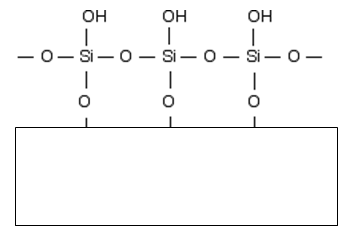
Silikagel je forma oxidu křemičitého, u kterého jsou atomy křemíku mezi sebou navázány přes molekuly kyslíku. Směrem k povrchu destičky jsou na atomy křemíku navázány –OH skupiny. Celá struktura pak vypadá následovně:
Navázané –OH skupiny dávají povrchu destičky polární vlastnosti s možností tvorby vodíkových můstků a dalších nekovalentních interakcí se separovanými látkami.
Mobilní fáze
Mobilní fáze je specificky definovaná směs rozpouštědel, kterou nalijeme v malé vrstvě (do 1 cm sloupce kapaliny) do chromatografické vany. Poté do vany vložíme chromatografickou desku s naneseným vzorkem tak, aby vzorek byl nad hladinou rozpouštědla a aby se TLC deska opírala o stěnu pouze zadní stranou. Mobilní fáze vzlíná po desce směrem vzhůru a unáší s sebou i analyzovaný vzorek. Rychlost, kterou je vzorek unášen směrem vzhůru, závisí na rozpustnosti vzorku v mobilní fázi a na stupni interakce s fází stacionární (afinitě k stacionární fázi). Čím větší je afinita vzorku ke stacionární fázi, tím pomaleji stoupá vzhůru. Když rozpouštědlo dorazí dostatečně daleko od startu (většinou více než do ¾ desky), vyjmeme desku z chromatografické vany a pozici na desce, kam doputovalo rozpouštědlo, označíme čarou (= čelo).
Retenční faktor
Poté změříme vzdálenost jednotlivých látek od startu a pro každou látku vypočítáme takzvaný retenční (retardační) faktor Rf. Hodnota Rf udává, jak daleko zaostává skvrna analyzované látky za čelem rozpouštědla. Rf je pro danou látku v daném systému charakteristický, tzn., že pokud experiment zopakujeme, měli bychom ve stejném uspořádání získat stejný Rf. V našem případě bude pro látku A , pro látku B (viz obrázek).
Postup
V tomto praktickém cvičení budeme používat plastovou destičku potaženou silikagelem. Celý postup by měl probíhat kvůli organické mobilní fázi v digestoři. Na aktivní stacionární fázi nesaháme, při manipulaci s deskou používáme rukavice.
- Nalijeme rozpouštědlo do chromatografické vany, uzavřeme ji víkem a necháme chvíli ekvilibrovat. Výpary rozpouštědla by měly vysytit vnitřní prostor nad hladinou.
- Pipetou nebo stříkačkou naneseme vzorek na TLC desku a nanesenou směs necháme uschnout.
- Odklopíme víko a desku vložíme co nejrychleji dovnitř. Víko ihned zaklopíme.
- Kontrolujeme, aby se čelo rozpouštědla nedostalo až za horní hranu desky. V tom případě by část vzorku "vyjela" ven a nebylo by možné určit Rf.
- Analýzu ukončíme vyjmutím desky z chromatografické vany a označením čela analýzy.
Je metoda separace (frakcionace) založená na rozdílné průchodnosti částic dělené směsi stacionární fází v závislosti na jejich velikosti.
Stacionární fáze je tvořena malými kuličkami, ve kterých je spousta „tunýlků“ a „jeskyněk“ o různé velikosti.
Některá složka dělené směsi však může mít tak velké částice, že se do žádné ze zmíněných prohlubenin nevejde, a tak má možnost pouze obtékat kuličky dělicího materiálu a protékat škvírami mezi nimi. Proto má při unášení mobilní fází k dispozici vlastně nejmenší prostor a je tak unášena nejrychleji.
Jiná složka může mít částice takové velikosti, že se již vejdou alespoň do některých otvůrků v kuličkách dělicího materiálu. Tak mají tyto částice při průtoku k dispozici nejen prostor okolo kuliček, ale i prostor prohlubenin dostatečné velikosti, kam mohou volně difundovat. Tím je jejich rychlost (při konstantním průtoku mobilní fáze, samozřejmě) o něco pomalejší než u velkých částic té první uvažované složky.
Konečně můžeme mít složku, jejíž částice jsou tak malé, že mají pro svůj pohyb k dispozici prostor všech otvůrků v kuličkách dělicího materiálu. Tato složka se proto bude ve směru průtoku mobilní fáze pohybovat nejpomaleji.
V konečném efektu tak teoreticky z chromatografické kolony vyteče jako první složka s největšími částicemi a jako poslední složka s nejmenšími částicemi. Proto slouží gelová permeační chromatografie pro dělení směsí vysokomolekulárních látek (hlavně bílkovin) podle jejich molekulových hmotností.
Nezbytnou podmínkou ale je, aby materiál dělicího média byl ke všem děleným složkám zcela inertní a specificky nezadržoval žádnou z nich.
Chceme-li rozdělit nějakou směs co nejlépe, musíme vybrat stacionární fázi s co nejvhodnějším rozsahem velikosti otvůrků. Takový výběr proto záleží na předpokládaném rozsahu velikosti (molekulové hmotnosti) složek dělené směsi. Naštěstí máme k dispozici velmi široké spektrum komerčních materiálů a běžně tak můžeme dělit směsi relativně nízkomolekulárních látek o molekulové hmotnosti řádu tisíců až desetitisíců daltonů i směsi velmi vysokomolekulárních látek s molekulovou hmotností statisíců až milionu.
Podle polarity stacionární a mobilní fáze rozlišujeme systémy hydrofilní a hydrofobní. V naprosté většině se však setkáváme s těmi prvními, tedy se systémy hydrofilními, a mezi nimi zcela převažuje systém polysacharidových skeletů stacionární fáze a vodných roztoků jako mobilní fáze.
Gelové permeační chromatografii se někdy říká nesprávně molekulární filtrace nebo filtrace na molekulových sítech. Jak vyplývá ze skutečné podstaty gelové permeační chromatografie, jsou to názvy zavádějící, protože se o žádnou filtraci nejedná.