Synapse
Synapse je specializovaný funkční kontakt mezi membránami dvou buněk, z nichž alespoň jedna je neuron. Funkcí synapse je přenos nervového vzruchu.
Typy synapsí[upravit | editovat zdroj]
Podle zúčastněných prvků dělíme synapse na:
- interneuronální:
- axo-dendritické;
- axo-somatické;
- dendro-dendritické;
- axo-axonální;
- somato-dendritické;
- neuroefektorové − např. nervosvalová ploténka (kontakt mezi axonem a svalovým vláknem);
- neuroreceptorové − mezi neuronem a receptorem.
Podle druhu přenosu signálu
- chemické
- elektrické
- smíšené
Synapse u člověka jsou nejčastěji synapse chemické, na kterých je signál přenášen prostřednictvím mediátoru (neurotransmiteru). Elektrické synapse jsou spíše vzácné, vyskytují se například v olivárních jádrech. Smíšené synapse nacházíme u nižších živočichů, jako jsou ryby.
Struktura elektrické synapse[upravit | editovat zdroj]
Elektrická synapse umožňuje přímý tok elektrického proudu, a proto se jedná o velmi rychlý (nejrychlejší) typ spojení. Je tvořena konexony, složenými ze šesti proteinů – konexinů, které společně vytváří spojení typu gap junction. Průtok otevřeným spojem je možný většinou obousměrně, u usměrněných synapsí pak probíhá napěťová regulace a dochází pouze k jednosměrnému vedení. Tento typ synapse je obvykle excitační.
Vzruch se přenese na postsynaptickou membránu pouze s mírným zmenšením amplitudy, protože jsou buňky propojeny úzkými konexony, což umožňuje průtok iontů, aniž by se otevíraly iontové kanály. U savců vzácně (olivární jádra, na glii), význam u studenokrevných.
Struktura chemické synapse[upravit | editovat zdroj]
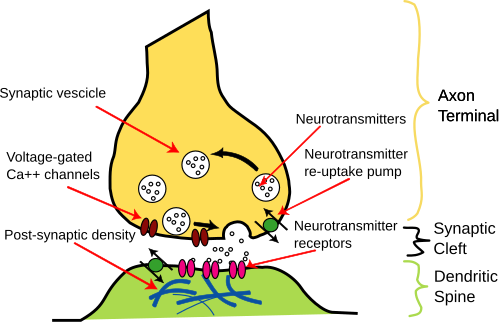
Chemické synapse jsou pomalým spojením, při procesu uvolňování mediátorů dochází ke zdržení minimálně o 0,5 ms. [1] Jsou zpravidla jednosměrné a mohou být jak excitační, tak inhibiční, podle typu uvolňovaného mediátoru. Synapsi tvoří presynaptický útvar a postsynaptický útvar, mezi nimiž je synaptická štěrbina (šířka štěrbiny je obvykle 20−30 nm [2], inhibiční synapse okolo 10 nm). Presynaptický útvar je buď zakončením axonu (tzv. terminální buton) nebo se jedná o vyklenutí axoplasmy axonu v jeho průběhu (synapse en passant). Presynaptická část je vakovité rozšíření axonu, které obsahuje synaptické váčky (vezikuly) a velké množství mitochondrií, které produkují ATP nutné při procesu uvolňování neurotransmiteru. Synaptické váčky obsahují molekuly mediátoru a hromadí se u synaptické štěrbiny v tzv. aktivní zóně synapse. Membrána postsynaptického útvaru obsahuje receptory pro mediátor.
Přenos vzruchu v synapsi[upravit | editovat zdroj]
Vzruch šířící se po axonu dosáhne presynaptického útvaru, čímž dochází k jeho depolarizaci (akční potenciál). Depolarizace způsobí otevření napěťově řízených Ca2+ kanálů v presynaptické membráně a influx Ca2+ do buňky. Vápenaté ionty uvolňují vazbu mezi proteiny cytoskeletu buňky a synaptickými váčky. Váčky jsou pomocí transportních proteinů ve své membráně (synaptobrevin, synaptotagmin) přesunovány do aktivní zóny. V aktivní zóně dochází ke splynutí transportních proteinů s proteiny na membráně neuronu (syntaxin, neurotaxin) a vzniká tzv. SNARE komplex. Obsah váčků je exocytózou uvolněn do synaptické štěrbiny (mediátor se uvolňuje v kvantech), probíhá vazba mediátoru na receptor postsynaptické membrány, čímž se v ní otevírají iontové kanály a dochází ke vzniku postsynaptických potenciálů.
Varianty receptorů[upravit | editovat zdroj]
Interakce mezi receptorem a iontovým kanálem může být různá. Iontové kanály v postsynaptické membráně, které se otevřou po vazbě mediátoru na receptor, patří mezi chemicky řízené iontové kanály (např. nikotinový acetylcholinový receptor). Receptor je bezprostřední součástí molekuly kanálu. Jiný způsob přenosu je spřažení receptoru s G-proteiny. Aktivuje se signalizační kaskáda přes adenylátcyklázu, druhého posla (cAMP) a proteinkinázu, která fosforylací docílí otevření iontového kanálu.
Odstranění mediátoru[upravit | editovat zdroj]
Po interakci mediátoru a receptoru musí být mediátor ze synaptické štěrbiny specifickým mechanismem odstraněn. To se děje nejčastěji dvěma cestami:
- přímý rozklad – v synaptické štěrbině se nachází enzymy rozkládající mediátor (např. acetylcholinesteráza);
- zpětné vychytávání – mediátor je vychytáván zpět do presynaptického zakončení a vrací se do synaptických vezikul (účast clathrinu a dynaminu) k opětovnému použití (noradrenergní, serotoninergní synapse,…).
Cholinergní synapse[upravit | editovat zdroj]
Popsaná jako 1. - Otto Loewi:
- nikotinové receptory: součást iontového kanálu; influx Na+;
- nebo může jít o muskarinové receptory: spřaženy s G-proteiny (metabotropní).
Acetylcholin je rozkládán acetylcholinesterázou - kotvena na presynaptické membráně, představuje regulaci uvolňování acetylcholinu. Následně je cholin reuptake cholinovým transportérem a cholinacetyltransferázou syntetizován znovu do podoby acetylcholinu, který je transportován do vezikul.
Adrenergní synapse[upravit | editovat zdroj]
Ligandem adrenergních synapsí jsou katecholaminy, zejména adrenalin a noradrenalin. Rozlišujeme tyto typy adrenergních receptorů:[3]
- α1-adrenergní receptory (podtypy α1A, α1B a α1D)
- α2-adrenergní receptory (podtypy α2A, α2B a α2C)
- β1-adrenergní receptory
- β2-adrenergní receptory
- β3-adrenergní receptory
Terapeutický význam má však jen dělení na α1, α2, β1 a β2 receptory. Všechny z nich jsou spřaženy G-proteiny.
Takové synapse nalezneme například v neuroefektorových synapsích sympatiku, kde se stýká axon postgangliového neuronu s efektorovou buňkou. S výjimkou potních žláz zde neuron používá jako neurotransmiter noradrenalin (v potních žlázách acetylcholin), který je uvolňován z vezikul do synaptické štěrbiny a váže se na receptory jak na efektorové buňce, tak na α2 receptory na neuronu, čímž zabraňuje dalšímu uvolňování noradrenalinu (zpětnovazebná inhibice).
Postsynaptické potenciály[upravit | editovat zdroj]
Postsynaptické potenciály závisí na druhu mediátoru a synapse. V organismu vznikají dva hlavní typy potenciálů:
- Excitační postsynaptický potenciál (EPSP) je způsoben excitačními mediátory. V postsynaptické membráně se otevírají Na+ (Ca2+) kanály a dochází ke vstupu iontů do buňky, což způsobí depolarizaci. Jeden EPSP představuje depolarizační změnu, která je hluboce podprahová (2−4 mV).[2] EPSP se ale sčítají (časová a prostorová sumace), takže může být dosaženo prahové úrovně (7,5-15 mV)[2], při které v eferentní části synapse vzniká akční potenciál;
- Inhibiční postsynaptický potenciál (IPSP) je způsoben inhibičními mediátory. Dochází k otevření K+ a Cl- kanálů a proudu kladných iontů ven z buňky a záporných do buňky. Membrána je pohyby iontů hyperpolarizována a snižuje se excitabilita neuronu. Hodnota IPSP je v rozmezí 2-5 mV.[2]
Kombinací EPSP a IPSP na stejné membráně dochází k součtu signálů. Pokud inhibiční signál dostatečně sníží excitační, nedochází ke vzniku akčního potenciálu.
Pomalé postsynaptické potenciály spočívají pouze v regulaci K+ kanálů. Při zvýšení propustnosti kanálů dochází k IPSP, při snížení vzniká EPSP. Tyto potenciály mají dlouhou latenci (100-500 ms)[4] a trvání (sekundy-minuty).[4]
Regulace přenosu vzruchu[upravit | editovat zdroj]
Presynaptická inhibice může probíhat dvěma způsoby. Prvním z nich je axo-axonální inhibice, při níž působí axon inhibičního neuronu na neuron presynaptický. Autoinhibice spočívá ve vazbě mediátoru na receptory vlastní presynaptické membrány, ze které je vyplavován. Dochází k útlumu dalšího uvolňování neurotransmiteru, což zabraňuje nadměrné stimulaci postsynaptické membrány.
Postsynaptická inhibice je taktéž možná pomocí inhibičního neuronu, který zde ovšem působí na neuron postsynaptický. Autoinhibice může probíhat aferentně kolatelárně - kolaterála z presynaptického neuronu aktivuje inhibiční interneuron, který inhibuje postsynaptický neuron. Eferentní kolaterální spoje vedou z postsynaptického neuronu přes inhibiční interneuron zpět na postsynaptický.
Presynaptická facilitace a sumace vzniká zejména když dva neurony konvergují na jeden. Podprahové podněty pak mohou vyvolat EPSP a následná sumace těchto signálů vyvolá akční potenciál. Nadprahové podněty vyvolají zpravidla prodloužený akční potenciál.
Okluze je zvláštním typem sumace, při níž dva nadprahové podněty vyvolají bežný akční potenciál (nikoli např. prodloužený, jako je tomu u presynaptické facilitace a sumace).
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
Použitá literatura[upravit | editovat zdroj]
- TROJAN, Stanislav, et al. Lékařská fyziologie. 4. vydání. Praha : Grada, 2003. 772 s. ISBN 80-247-0512-5.
- KITTNAR, Otomar, et al. Lékařská fyziologie. 1. vydání. Praha : Grada, 2011. ISBN 978-80-247-3068-4
- MYSLIVEČEK, Jaromír a A KOL.. Základy neurověd. 2. vydání. Praha : Triton, 2009. 390 s. s. 38. ISBN 978-80-7387-088-1.
Reference[upravit | editovat zdroj]
- ↑ KITTNAR, Otomar a ET AL.. Lékařská fyziologie. 1. vydání. Praha : Grada, 2011. 790 s. s. 76. ISBN 978-80-247-3068-4.
- ↑ a b c d TROJAN, Stanislav a ET AL.. Lékařská fyziologie. 4. vydání. Praha : Grada, 2003. 772 s. s. 65–67. ISBN 80-247-0512-5.
- ↑ LÜLLMANN, Heinz, Klaus MOHR a Lutz HEIN, et al. Barevný atlas farmakologie : Překlad 5., přepracovaného a rozšířeného vydání. 3. vydání. Praha : Grada Publishing a.s., 2007. ISBN 978-80-247-1672-5.
- ↑ a b MYSLIVEČEK, Jaromír a A KOL.. Základy neurověd. 2. vydání. Praha : Triton, 2009. 390 s. s. 38. ISBN 978-80-7387-088-1.