Nejvýznamnější chemické reakce v metabolismu
Metabolické dráhy lidského organismu tvoří rozsáhlou síť propojených reakcí, které často sdílejí společné meziprodukty. Chemické přeměny jednotlivých látek obvykle třídíme podle určitého obecného mechanismu společného pro všechny látky podstupující danou reakci. Například u dekarboxylace se jedná o odštěpení CO2 z karboxylové skupiny, přičemž substrátem mohou být různé karboxylové kyseliny.
Alkoholy, karbonylové sloučeniny a karboxylové kyseliny[upravit | editovat zdroj]
Alkoholy, karbonylové sloučeniny a karboxylové kyseliny patří mezi významné substráty mnoha reakcí metabolických drah organismů.
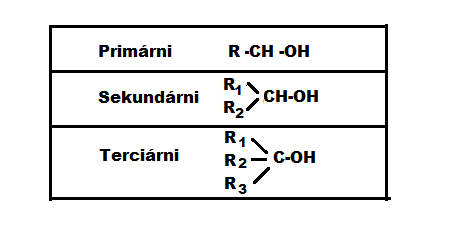
Alkoholy obsahují funkční skupinu −OH. Podle počtu OH skupin v molekule mohou být alkoholy jedno-, dvou- nebo vícesytné. Dále podle toho, na jaký atom uhlíku se −OH skupina váže, rozlišujeme primární, sekundární a terciární alkoholy.
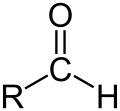
Aldehydy s ketony tvoří skupinu karbonylových sloučenin. Funkční skupinou aldehydů je skupina −CHO, u ketonů −C=O. Z této skupiny látek jsou pravděpodobně nejvýznamnějšími substráty reakcí karboxylové kyseliny, charakterizované přítomností funkční skupiny −COOH, a jejich deriváty.
Významné reakce alkoholů, aldehydů a karboxylových kyselin[upravit | editovat zdroj]
- Tvorba aniontů a acylů odvozených od karboxylových kyselin
- Dehydrogenace a hydrogenace (oxidace a redukce)
- Esterifikace
Tvorba aniontů a acylů odvozených od karboxylových kyselin[upravit | editovat zdroj]
Karboxylová skupina je schopna disociace, přičemž míru disociace pro jednotlivé kyseliny udává disociační konstanta. Karboxylové kyseliny patří mezi kyseliny slabé, což znamená, že jejich disociace je jen parciální. Z kyseliny tak vzniká anion (skupina −COO−). Po odštěpení celé −OH skupiny z karboxylové skupiny vzniká její acyl.
Dehydrogenace a hydrogenace (oxidace a redukce)[upravit | editovat zdroj]
Během chemické reakce, dehydrogenace, dochází k odstranění −H z molekuly. Získaný vodík, můžeme následně využít při tvorbě protonového gradientu v mitochondriích a k zisku energie (ATP). Vnesení vodíku do molekuly se nazývá hydrogenace. V organismu se dehydrogenace a hydrogenace vyskytují například v těchto pochodech:
- Oxidace jednoduchých vazeb na vazby dvojné
-
- −CH2−CH2− −CH=CH− + 2 H+ + 2 e−
- Tyto reakce se vyskytují například v Krebsově cyklu, při β-oxidaci mastných kyselin či desaturačních reakcích, které mají za cíl syntézu nenasycených MK.
- Vzájemné přeměny alkoholů, aldehydů / ketonů a karboxylových kyselin
- Alkoholy, karbonylové sloučeniny a karboxylové kyseliny tvoří řadu vzájemně se lišící stupněm oxidace / redukce.
- Obecné schéma jejich vzájemné přeměny je následující (směrem ke karbonylové sloučenině a karboxylové kyselině probíhá oxidace, směrem opačným redukce):
- Primární alkohol aldehyd karboxylová kyselina
- R−CH2−OH R−CHO R−COOH
- Sekundární alkohol keton
- R1−CH(OH)−R2 R1−CO−R2
- Terciární alkohol
- „Mírná“ oxidace neprobíhá (lze oxidovat až za současného štěpení uhlíkového řetězce).
Jako příklad oxidace nám může posloužit vznik dihydroxyacetonfosfátu (DHA-P) z glycerol-3-fosfátu (kofaktorem je FAD), přes který vstupuje glycerol dle aktuálních potřeb organismu do glykolýzy či do glukoneogeneze.
Esterifikace[upravit | editovat zdroj]
Esterifikace je reakce karboxylové kyseliny s alkoholem, při které vzniká ester a voda:
Nejvýznamnější karboxylové kyseliny, jejich anionty a acyly[upravit | editovat zdroj]
Nasycené monokarboxylové kyseliny[upravit | editovat zdroj]
| C | Systematický název | Triviální název | Latinský název | Acyl | Anion |
|---|---|---|---|---|---|
| 1 | metanová | mravenčí | ac. formicum | formyl | formiát |
| 2 | etanová | octová | ac. aceticum | acetyl | acetát |
| 3 | propanová | propionová | ac. propionicum | propionyl | propionát |
| 4 | butanová | máselná | ac. butyricum | butyryl | butyrát |
| 5 | pentanová | valérová | ac. valericum | valeryl | valerát |
| 12 | dodekanová | laurová | ac. lauricum | lauryl | laurát |
| 16 | hexadekanová | palmitová | ac. palmiticum | palmitoyl | palmitát |
| 18 | oktadekanová | stearová | ac. stearicum | stearoyl | stearát |
Nasycené dikarboxylové kyseliny[upravit | editovat zdroj]
| C | Systematický název | Triviální název | Latinský název | Acyl | Anion |
|---|---|---|---|---|---|
| 2 | etandiová | štavelová | ac. oxalicum | oxalyl | oxalát |
| 3 | propandiová | malonová | ac. malonicum | malonyl | malonát |
| 4 | butandiová | jantarová | ac. succinicum | sukcinyl | sukcinát |
| 5 | pentandiová | glutarová | ac. glutaricum | glutaryl | glutarát |
| 6 | hexandiová | adipová | ac. adipicum | adipoyl | adipát |
Nenasycené monokarboxylové kyseliny[upravit | editovat zdroj]
| C | Systematický název | Triviální název | Latinský název | Acyl | Anion |
|---|---|---|---|---|---|
| 18:1 | cis-oktadec-9-enová | olejová | ac. oleicum | oleoyl | oleát |
| 18:2 (ω−6) | cis,cis-oktadeka-9,12-dienová | linolová | ac. linoleicum | linoloyl | linolát |
| 18:3 (ω−3) | cis,cis,cis-oktadeka-9,12,15-trienová | linolenová | ac. linolenicum | linolenoyl | linolenát |
| 20:4 (ω−6) | cis,cis,cis,cis-eikosa-5,8,11,14-tetraenová | arachidonová | ac. arachidonicum | arachidonyl | arachidonát |
Nenasycené dikarboxylové kyseliny[upravit | editovat zdroj]
| C | Systematický název | Triviální název | Latinský název | Acyl | Anion |
|---|---|---|---|---|---|
| 4 | cis-butendiová | maleinová | ac. maleicum | maleinyl | maleinát |
| 4 | trans-butendiová | fumarová | ac. fumaricum | fumaroyl | fumarát |
Deriváty karboxylových kyselin[upravit | editovat zdroj]
| C | Systematický název | Triviální název | Latinský název | Acyl | Anion |
|---|---|---|---|---|---|
| 3 | 2-oxopropanová | pyrohroznová | ac. pyruvicum | pyruvyl | pyruvát |
| 3 | 2-hydroxypropanová | mléčná | ac. lacticum | laktoyl | laktát |
| 4 | 3-oxobutanová | acetooctová | acetoacetyl | acetoacetát | |
| 4 | 3-hydroxybutanová | β-hydroxymáselná | β-hydroxybutyrát | ||
| 4 | 2-hydroxybutandiová | jablečná | ac. malicum | maloyl | malát |
| 4 | 2-oxobutandiová | oxaloctová | oxalacetát | ||
| 5 | 2-oxopentandiová | α-ketoglutarová | α-ketoglutaryl | α-ketoglutarát | |
| 6 | 2-hydroxypropan-1,2,3-trikarboxylová | citrónová | ac. citricum | citrát |
Hydroxykyseliny a ketokyseliny[upravit | editovat zdroj]
Hydroxykyseliny kromě skupiny −COOH obsahují i −OH skupinu nahrazující jeden −H. Ketokyseliny čili oxokyseliny obsahují v molekule kromě skupiny −COOH i skupinu =O nahrazující jeden −H. Jejich vzájemná přeměna je v metabolických drahách relativně běžná.
Jako příklad poslouží v metabolismu relativně častá keto-enol tautomerie. Dochází při ní k přeměně dvou forem organických sloučenin:
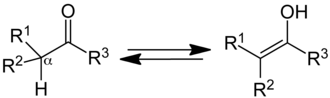
- ketoforma (či také oxoforma) obsahuje dvojnou vazbou vázaný kyslík jako skupinu =O,
- enolforma, která obsahuje dvojnou vazbu mezi uhlíky a na jeden z nich se váže −OH skupina (tj. obsahuje strukturu R1−CH=C(OH)−R2).
Vzájemná přeměna obou forem představuje migraci atomu vodíku či protonu, provázenou prohozením jednoduché vazby a k ní přiléhající vazby dvojné.
Aminokyseliny a oxokyseliny[upravit | editovat zdroj]
Aminokyseliny a oxokyseliny představují substituční deriváty karboxylových kyselin. Aminokyseliny obsahují v molekule kromě −COOH skupiny i skupinu −NH2, oxokyseliny skupinu =O. Jejich vzájemné přeměny jsou v organismu časté, dochází při nich např. k záměně −NH2 skupiny za skupinu =O a naopak.
K těmto přeměnám dochází především při dvou dějích:
- Transaminace
- Při této reakci je aminokyselina donorem −NH2 skupiny pro oxokyselinu. Z příslušné oxokyseliny vzniká aminokyselina a původní aminokyselina se stává oxokyselinou:
- AK1 + OxoK2 OxoK1 + AK2
- Oxidační deaminace
- Jedná se o vznik oxokyseliny z aminokyseliny odstraněním −NH2 skupiny, jež se uvolňuje jako amoniak (NH3). Oxidační deaminace patří k významným reakcím, skrze které zahajují aminokyseliny proces svého odbourávání. V lidském těle probíhají zejména v játrech a uvolněný amoniak se odbourává při syntéze močoviny.
- Uvedenou reakci katalyzuje především glutamátdehydrogenáza.
Dekarboxylace a karboxylace[upravit | editovat zdroj]
Při dekarboxylaci dochází k odstranění karboxylové skupiny, která se uvolní v podobě molekuly CO2 a je nahrazena protonem. Jsou významné např. pro
- přeměny aminokyselin na biogenní aminy (např. při syntéze mnoha neurotransmiterů),
- dehydrogenace 2-ketokyselin – pyruvátdehydrogenázová reakce a dvě reakce Krebsova cyklu.
Karboxylace je reakce opačná, dochází při ní k vnesení −COOH skupiny do molekuly. Vyskytuje se například při
- syntéze mastných kyselin,
- glukoneogenezi.