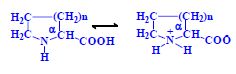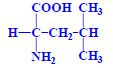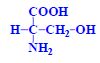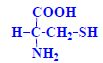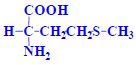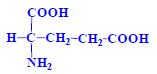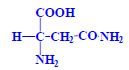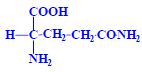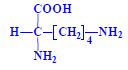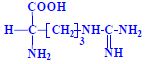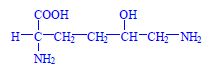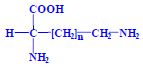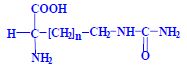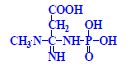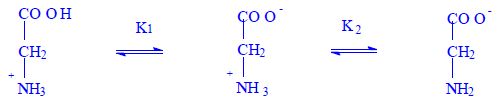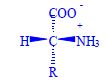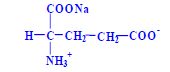Chemie živin
Náplň podkapitoly
Přehled živin – sacharidy
Klasifikace a struktura
Sacharidy, také nazývané glycidy, jsou nejrozšířenější organické látky na Zemi. Jejich molekuly tvoří atomy kyslíku, uhlíku a vodíku. Z chemického hlediska se jedná o polyhydroxyaldehydy a polyhydroxyketony. Ve své molekule obsahují funkční aldehydové nebo ketoskupiny, a také větší počet hydroxylových skupin.
Klasifikace sacharidů
Podle počtu jednotek v molekule
- monosacharidy – nemohou být dále hydrolyzovány na jednodušší jednotky;
- oligosacharidy – hydrolýzou vytvoří 2–10 jednotek monosacharidů;
- polysacharidy – hydrolyzující se na více než 10 monosacharidů.
Monosacharidy
- Počtu C-atomů: triózy, tetrózy, pentózy, hexózy.
- Funkční skupiny: aldózy a ketózy.
Polysacharidy
- Homopolysacharidy: jedná se o polymery tvořené stejným druhem monosacharidu. Příkladem je škrob, glykogen či celulóza.
- Heteropolysacharidy: jsou to polymery tvořené více než jedním typem monosacharidu. Příkladem je hemicelulóza.
Struktura sacharidů
Pro zápis můžeme využívat různé druhy vzorců:
- Lineární (Fischerův) vzorec;
- Cyklický (Hawortův) vzorec, který vzniká vytvořením heterocyklické struktury.
- Tollensův vzorec popisuje tvorbu cyklické struktury ze vzorce lineárního. Ukazuje reakci hydroxylu s karbonylovou skupinou za vzniku tzv. poloacetalové (hemiacetalové) struktury.
Cyklus může být:
- šestičlenný – pyranóza – podle podobnosti se šestiuhlíkatým pyranem;
- pětičlenný – furanóza – podle podobnosti s pětiuhlíkatým furanem.
Izomerie
Je to stav, kdy mají sloučeniny se stejným sumárním vzorcem jiné strukturní uspořádání atomů v molekule. U molekul sacharidů se setkáváme s následujícími druhy izomerie.
- D- a L- řada
- Označuje se podle pozice −OH skupiny na posledním chirálním uhlíku. Přiřazení k příslušné řadě vychází z podobnosti s výchozí sloučeninou sacharidové řady – glyceraldehydem. Skupina −OH se ve Fischerově vzorci nachází vpravo pro D- a vlevo pro L- izomery.
- D- a L- izomery jsou zrcadlovými obrazy tzv. enantiomery – optické izomery. Liší se znaménkem optické otáčivosti, neboli směru, ve kterém otáčejí rovinu polarizovaného světla.
- Neplatí však obecně, že by D- řada byla pravotočivá a L- řada levotočivá.
- Ekvimolární směs enantiomerů se nazývá racemická směs, nebo také DL směs, a optickou aktivitu nevykazuje.
- V přírodě se vyskytují častěji D- izomery .
Pyranózy a furanózy
- Označují se podle podobnosti cyklické formy příslušného monosacharidu s cyklem pyranu nebo furanu. Glukóza v roztoku se vyskytuje z více než 99 % ve formě gluko-pyranózy, zbylá část molekul, méně než 1 %, se pak objevuje ve formě gluko-furanózy.
α- a β- anomery
- Označují se podle polohy hemiacetálového nebo hemiketalového −OH v cyklu. Hemiacetaly vznikají reakcí aldehydové a alkoholové skupiny, hemiketaly reakcí keto- a alkoholové skupiny.
- Pokud je −OH skupina orientována na stejnou stranu jako −OH skupina označující příslušnost k D- nebo L- řadě, jde o α-anomer. Pokud je −OH skupina orientována na stranu protilehlou, jedná se o β-anomer.
Anomery se liší optickou otáčivostí.
Epimery
- Liší se od sebe polohou jedné −OH skupiny v molekule.
Příkladem jsou glukóza a manóza.
Aldózy a ketózy
- Označují se podle odlišné funkční skupiny na 1. a 2. uhlíku molekuly.
Význam pro tělo
Sacharidy nejsou pro tělo esenciální a běžně se v něm syntetizují, např. z aminokyselin nebo glycerolu.
- Monosacharidy a disacharidy představují důležitý zdroj energie. Jsou nezbytné zejména pro buňky mozku a erytrocyty.
- Polysacharidy slouží jako zásobárna energie – glykogen u živočichů.
Sacharidy plní i strukturní funkce, například jako součást glykoproteinů a glykolipidů v membránách.
Klíčovou roli hrají i při syntéze nukleových kyselin nebo koenzymů. Jsou též součástí mezibuněčné hmoty, například v molekulách proteoglykanů.
Přehled sacharidů
Monosacharidy a disacharidy
- Jedná se o bílé krystalické látky rozpustné ve vodě, neutrální povahy, které ve vodných roztocích nedisociují. Mají polární charakter a −OH skupiny způsobují jejich sladkou chuť i silnou hydrataci v roztoku.
- Nejdůležitějšími monosacharidy v potravě jsou glukóza, fruktóza a galaktóza. Z disacharidů sacharóza α-Glc (1→2) β-Fru používaná jako sladidlo, řepný cukr, laktóza, β-Gal (1→4) β-Glc, přítomná v mléce a maltóza, α-Glc (1→4) β-Glc, přítomná ve sladu.
Cukerné alkoholy
- Cukerné alkoholy vznikají redukcí karbonylové skupiny na skupinu hydroxylovou. Například glucitol, neboli sorbitol, který vzniká redukcí glukózy či fruktózy.
Polyhydroxyderiváty karboxylových kyselin
- Vznikají oxidací monosacharidů. Při oxidaci slabým činidlem se oxiduje aldehydová skupina a vytvářejí se aldonové kyseliny. Silnější činidla oxidují nejen aldehydovou skupinu, ale i primární −OH skupiny na konci molekuly, takže vznikají dikarboxylové aldarové kyseliny. Oxidace pouze primární −OH skupiny aldóz v těle probíhá enzymaticky za vzniku uronových kyselin. Například z glukózy vzniká glukuronová kyselina, významné konjugační činidlo v játrech, které napomáhá vylučování ve vodě špatně rozpustných látek.
Deoxycukry
- Vznikají redukcí hydroxylové skupiny sacharidu. Příkladem je deoxyribóza, důležitá složka nukleových kyselin.
Aminocukry
- Vznikají náhradou hydroxylové skupiny za skupinu −NH2. Mezi důležité aminocukry v organismu patří například D-glukosamin, součást molekul mezibuněčné hmoty.
Estery
- Vznikají esterifikací hydroxylové skupiny H3PO4. Například vznik glukóza-6-fosfátu z molekuly glukózy. Nebo H2SO4 součásti proteoglykanů.
Glykosidy
Vznikají reakcí hydroxylové skupiny s:
- Alkoholem – vznik O-glykosidické vazby. Například vznik di- a polysacharidů, či vazba monosacharidů na proteiny přes aminokyseliny serin a threonin.
- Aminem – vznik N-glykosidické vazby. Příkladem je vazba na proteiny přes aspartát nebo vazba ribózy v nukleotidech.
- Nejreaktivnější skupinou v molekule monosacharidu je anomerní skupina −OH.
- Neredukujíci disacharidy vznikají pokud se glykosidická vazba vytvoří mezi anomerními hydroxyly obou monosacharidů, jako například u sacharózy. Disacharid nereaguje s oxidačním činidlem.
- Redukující disacharid vzniká reaguje-li anomerní hydroxyl jednoho monosacharidu s jiným než anomerním hydroxylem druhého monosacharidu. Volné aldózy, monosacharidy, jsou redukující všechny, z disacharidů jsou redukující například laktóza či maltóza.
Polysacharidy a vláknina
- Polysacharidy bývají látky amorfní a jsou buď ve vodě nerozpustné, nebo tvoří koloidní roztoky. Obecně se označují jako glykany. Mohou být tvořeny jen jedním typem monosacharidu, například glukózou jako u škrobu a glykogenu. Tyto polysacharidy pak označujeme jako glukany. Pokud monosacharid bude fruktóza, nazýváme tento polysacharid fruktan. Nebo jsou tvořeny různými monosacharidy a jejich deriváty, jako jsou glykosaminoglykany.
- Zásobní polysacharidy jako škrob či glykogen jsou ve vodě částečně rozpustné, zatímco strukturní polysacharidy jako celulóza mají v struktuře mnoho intra- a intermolekulárních vodíkových můstků a jsou ve vodě nerozpustné.
Vláknina
- Tvoří ji heterogenní skupina strukturních polysacharidů, které lidské enzymy nedokáží rozštěpit, a proto je nevstřebatelnou součástí potravy. Pro trávení je ovšem velmi důležitá – zvyšuje objem tráveniny, což urychluje střevní peristaltiku a škodlivé látky tak zůstávají v trávicím traktu kratší dobu. Současně na sebe váže některé cizorodé i endogenní látky, čímž zvyšuje jejich vylučování z organismu. Toto platí například pro žlučové kyseliny tvořené z cholesterolu – konzumace vlákniny tedy snižuje množství cholesterolu v organismu.
Vlákninu dělíme:
- Rozpustnou vlákninu (hemicelulóza, pektiny).
- Je štěpena bakteriemi tlustého střeva na mastné kyseliny s krátkým řetězcem, kyselina octová, propionová, máselná, jež jsou významným zdrojem energie pro kolonocyty.
- Nerozpustnou vlákninu (celulóza).
- Celulózu nedokážou rozštěpit ani bakteriální enzymy a z těla odchází nestrávená. Její význam spočívá ve zvyšování objemu tráveniny a podpoře peristaltických pohybů.
Heteroglykosidy
- Látky obsahující kromě sacharidové části (glykonu) i jiný typ sloučenin (aglykony) se nazývají heteroglykosidy. Patří sem:
- Proteoglykany
- Obsahují lineární dlouhé polysacharidové řetězce vázané na protein. Řetězce jsou tvořeny střídáním hexózaminu s uronovou kyselinou a označují se jako glykosaminoglykany (GAG).
- Glykoproteiny
- Glykoproteiny, čili proteiny na různých místech glykosylováné (O– nebo N– glykosidickou vazbou) krátkými větvenými molekulami oligosacharidů, na rozdíl od proteoglykanů neobsahují uronové kyseliny.
- Glykolipidy
- Glykolipidy, látky lipidové povahy mají v molekule jednu nebo několik monosacharidových jednotek.
Přehled živin – Lipidy
Klasifikace a struktura lipidů
Pro lipidy, skupinu chemicky i funkčně heterogenních látek, je společná nerozpustnost ve vodě – hydrofobnost, výborná rozpustnost v nepolárních rozpouštědlech a přítomnost alkoholů a mastných kyselin v molekule. V organizmu jsou často syntetizovány z acetyl-CoA.
Mastnými kyselinami se obvykle rozumí vyšší monokarboxylové kyseliny. Obsahují přibližně 8 a více atomů uhlíku, s typicky sudým počtem uhlíkových atomů (protože vznikají z acetyl-CoA). Pokud obsahují dvojné vazby, jsou zpravidla izolované a v cis-konfiguraci. Převahu mají kyseliny s délkou C16 a C18.
Klasifikace lipidů
Jednoduché lipidy
- Acylglyceroly
- Vosky
Složené lipidy
- Fosfolipidy
- Glycerolfosfolipidy
- Sfingolipidy
- Glykolipidy
- Cerebrosidy
- Gangliosidy
- Lipoproteiny
Jednoduché lipidy
Jednoduché lipidy jsou estery mastných kyselin a alkoholů. Jsou tvořené jen hydrofobní částí.
Acylglyceroly
Acylglyceroly (glyceridy) jsou estery vyšších mastných kyselin a glycerolu. Podle počtu molekul mastných kyselin navázaných na alkohol je dělíme na mono-, di- nebo triacylglyceroly. Největší význam pro nás mají triacylglyceroly, které jsou součást tuků – směsi tuhých triacylglycerolů, nebo olejů – směsi kapalných triacylglycerolů.
Kyselou hydrolýzou acylglycerolů zpětně vznikají příslušné mastné kyseliny a glycerol.
Alkalickou hydrolýzou, zmýdelněním, vzniká glycerol a směs solí mastných kyselin – mýdla.
Vosky
Vosky jsou estery vyšších mastných kyselin a vyšších jednosytných alkoholů. Příkladem může být cetylalkohol s šestnácti uhlíkovými atomy, cerylalkohol s dvaceti šesti uhlíky nebo myricylalkohol s třiceti atomy uhlíku.
Složené lipidy
Složené lipidy tvoří základní stavební prvek buněčných membrán. Řadíme mezi ně fosfolipidy, glykolipidy a lipoproteiny. Složené lipidy obsahují kromě hydrofobní části i složky hydrofilní. Označují se proto jako polární lipidy a tvoří micely a dvojvrstvy.
Fosfolipidy
Fosfolipidy obsahují ve své molekule zbytek kyseliny fosforečné H3PO4. Mezi fosfolipidy řadíme glycerolfosfolipidy a sfingofosfolipidy.
Glycerolfosfolipidy (fosfoacylglyceroly)
Základem glycerolfosfolipidů je molekula kyseliny fosfatidové, kterou tvoří glycerol esterifikovaný dvěma molekulami mastných kyselin a jednou molekulou H3PO4. Na fosfátovou skupinu kyseliny fosfatidové se může vázat další složka, např. cholin, serin, etanolamin apod. Nejpočetnější skupinou glycerolfosfolipidů jsou fosfatidylcholiny (lecitiny) a uplatňují se jako součást biologických membrán.
Sfingofosfolipidy
Sfingofosfolipidy obsahují alkohol sfingosin, na který se váží další složky.
- Sfingosin s navázanou mastnou kyselinou se nazývá ceramid.
- Nejvýznamnější podskupinou jsou sfingomyeliny tvořené ceramidem s navázaným zbytkem kyseliny fosforečné a cholinem. Sfyngomyeliny se vyskytují například v nervové tkáni.
Glykolipidy
Glykolipidy obsahují jeden nebo více monosacharidů. Tyto monosacharidy jsou glykosidicky vázané na lipidovou součást molekuly mono- či diacylglycerolu nebo sfingosinu. Mezi glykolipidy řadíme cerebrosidy a gangliosidy.
- Cerebrosidy jsou tvořeny molekulou ceramidu s navázanou galaktózou. Vyskytují se zejména v bílé hmotě CNS. Na cerebrosidy se může vázat H2SO4, pak je nazýváme sulfatidy.
- Gangliosidy jsou tvořeny ceramidem, na který je navázaný oligosacharid, obvykle galaktóza a glukóza. Vyskytují se v gangliích nervových buněk a šedé hmotě CNS.
Lipoproteiny
Lipoproteiny jsou tvořeny kombinací lipidů a proteinů.
.
Esenciální mastné kyseliny
- Lidský organismus dokáže molekulu mastné kyseliny desaturovat maximálně na pozici 9. uhlíku.
- Pokud se dvojná vazba nachází dále, tělo ji vytvořit neumí a takové mastné kyseliny musíme přijímat v potravě a nazýváme je esenciální mastné kyseliny.
Kyselina linolová
- Kyselina linolová je tvořena osmnácti uhlíky a dvěma dvojnými vazbami. Cis dvojné vazby jsou v polohách 9 a 12, a proto je označována jako ω-6.
- Nachází se především v rostlinných olejích, například slunečnicovém. Má prozánětlivé účinky, stejně jako jiné ω-6 mastné kyseliny, a zvyšuje hladiny některých lipidů v plazmě.
- Kyselina linolová se využívá při biosyntéze kyseliny arachidonové.
Kyselina arachidonová
- Kyselina arachidonová je tvořena dvaceti uhlíky a čtyřmi dvojnými vazbami, také se jedná o ω-6 mastnou kyselinu. Funguje jako důležitý prekurzor biologicky aktivních látek – eikosanoidů (prostaglandiny, prostacykliny, leukotrieny a tromboxany).
Kyselina α-linolenová
Kyselinu α-linolenovou tvoří osmnáct uhlíků a tři dvojné vazby. Cis dvojné vazby se nachází v polohách 9, 12 a 15, proto je označována jako ω-3. Nachází se především v rybách a mořských živočiších. Snižuje hladinu cholesterolu a TAG v těle a snižuje tak riziko kardiovaskulárních onemocnění, má i protizánětlivé účinky.
Význam lipidů pro tělo
- Lipidy jsou nejredukovanější, a tedy energeticky nejbohatší živinou. Uplatňují se tak jako významný energetický substrát. Některé tkáně, jako např. mozek, je však v metabolismu běžně nedovedou využít. Pro svou hydrofobnost, díky které nevážou na rozdíl od sacharidů vodu, jsou nejefektivnější zásobárnou energie.
- Další funkce
- Strukturní funkce – tvoří například nezbytnou složku všech buněčných membrán.
- Mechanická a ochranná funkce – podkožní tuk a tuk kolem orgánů izoluje tepelně a fyzikálně, myelinové pochvy neuronů izolují elektricky.
- Významná rozpouštědla některých látek (vitaminy rozpustné v tucích) a jsou výchozí látkou pro syntézu mnoha pro tělo významných látek – eikosanoidy, steroidní hormony, žlučové kyseliny apod.
Izoprenoidy
- V organismu se nachází skupina látek, jejichž struktura se odvozuje od molekuly izoprenu – tvoří je dvě či více izoprenových jednotek.
- Steroidy, deriváty triterpenoidů, obsahují šest izoprenových jednotek. Nejdůležitější zástupce steroidů, cholesterol, tvoří součást buněčných membrán, jeho deriváty (žlučové kyseliny, steroidní hormony) pak plní v organismu mnoho důležitých funkcí.
Přehled živin – proteiny
Klasifikace a struktura proteinů
- Proteiny jsou makromolekulární organické látky tvořené řetězcem aminokyselin vzájemně spojených peptidovou vazbou. Ta spojuje jednoduchou kovalentní vazbou aminoskupinu jedné aminokyseliny a karboxylovou skupinu druhé aminokyseliny. Polykondenzací vzniká různě dlouhý řetězec aminokyselin ukončený na jedné straně volnou aminoskupinou, N-konec, a na straně opačné volnou karboxylovou skupinou, C-konec.
- Peptidy představují oproti proteinům kratší řetězce aminokyselin (méně než 100) a mají molekulovou hmotnost pod 10 000.
Klasifikace proteinů
- Proteiny můžeme dělit na dvě základní skupiny podle složení.
Jednoduché proteiny
Jednoduché proteiny obsahují řetězce tvořené jen aminokyselinami. Rozlišujeme:
- Fibrilární proteiny – skleroproteiny
- Fibrilární proteiny, ve vodě nerozpustné, plní zejména strukturní funkce. Jednotlivé peptidové řetězce jsou vzájemně propojeny příčnými vazbami tak, že tvoří paralelně probíhající vlákna. Příkladem fibrilárních proteinů jsou kolagen či keratin, vyskytující se v chlupech, kůži či nehtech.
- Globulární proteiny – sféroproteiny
- Řetězec globulárních proteinů má kulovitý tvar umožňující zabalení hydrofobních částí molekuly dovnitř. Jsou proto ve vodě rozpustné, např. albumin.
Složené proteiny
Složené proteiny obsahují kromě proteinové části i jinou neproteinovou strukturu. Rozlišujeme:
- Glykoproteiny – obsahující glykosidicky vázaný sacharid;
- Metaloproteiny – obsahující iont kovu (Fe, Cu), například ferritin nebo transferrin;
- Chromoproteiny – obsahující jako prostetickou skupinu pigment, například hemoglobin, cytochromy či myoglobin;
- Nukleoproteiny – obsahující navázané nukleové kyseliny;
- Lipoproteiny – obsahující lipidy.
Struktura proteinů
V molekule proteinů můžeme rozlišit několik struktur:
Primární struktura
- Primární struktura je podmíněna sekvencí aminokyselin v řetězci bílkoviny. Jejich pořadí čteme od N- k C-konci. Aminokyseliny řetězce jsou vzájemně spojeny peptidovými vazbami.
Sekundární struktura
- Sekundární struktura je podmíněna vznikem vodíkových můstků mezi NH– a C=O skupinami peptidové vazby. Mezi nejčastější sekundární struktury patří alfa-helix a beta-skládaný list.
- Alfa-helix
- Řetězec bílkoviny je stočen do pravotočivé nebo levotočivé šroubovice s délkou jednoho závitu 3,6 aminokyselinových zbytků. Postranní řetězce vyčnívají směrem ven ze šroubovice.
- Beta-skládaný list
- Řetězce jsou dva, uspořádané rovnoběžně a antiparalelně. Vzájemně je stabilizují H-můstky.
- Kromě těchto dvou sekundárních struktur se vyskytuje i mnoho jiných, například Zn-prst nebo Leu-zip.
Terciární struktura
- Terciární struktura popisuje prostorové uspořádání molekuly podmíněné interakcemi mezi vedlejšími skupinami řetězce – elektrostatickými silami, H-můstky, SH-vazbami, nepolárními interakcemi apod.
Kvarterní struktura
- Kvarterní struktura popisuje prostorové uspořádání podjednotek proteinů složených z více než jednoho řetězce. Podjednotky nejsou vzájemně spojeny peptidovými vazbami.
- Denaturace je děj, při kterém dochází k narušení všech vyšších struktur proteinu kromě primární. Protein ztrácí svou funkčnost, jeho energetická hodnota ale zůstává zachována. Mezi příčiny mohou náležet vysoká teplota, změna pH nebo přítomnost solí těžkých kovů.
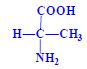
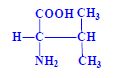
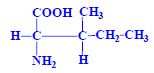
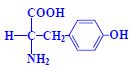
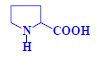
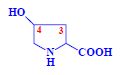
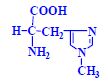
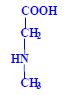
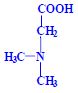
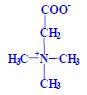
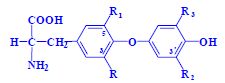
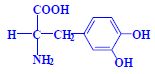
Aminokyseliny
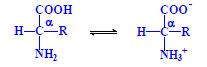
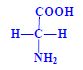
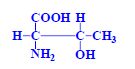
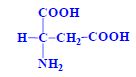
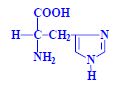
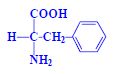
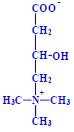
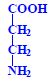
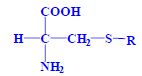
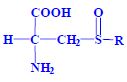
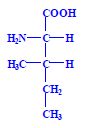
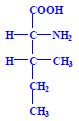
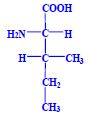
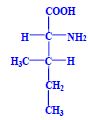
Aminokyseliny jsou základní stavební jednotky proteinů. Chemicky jsou to organické sloučeniny navzájem spojené peptidovou vazbou. V aminokyselině musí být přítomna alespoň jedna primární aminoskupina –NH2 a současně alespoň jedna karboxylová skupina –COOH. Chemicky jsou to substituční deriváty karboxylových kyselin.
- 2–100 aminokyselin (monomerů) – peptidy
- 100 a více aminokyselin – proteiny
V přírodě bylo prokázáno více než 700 různých AMK. Proto také rozdělujeme AMK dle jejich výskytu:
- aminokyseliny nacházející se ve všech živých organismech
- vázané v bílkovinách (21 proteinogenních AMK), peptidech nebo jako volné AMK
- aminokyseliny nacházející se jen v některých organismech
- vázané v peptidech nebo jako volné AMK
- nejsou složkami bílkovin
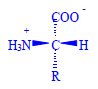
Proteinogenní aminokyseliny, nebo-li také kódované, se vyskytují v bílkovinách jako L-alfa-aminokyseliny (výjimkou je glycin). Je to dáno chemickým uspořádáním, které je nezbytné pro biogenní funkci. Konkrétní druhy aminokyselin, jejich posloupnost a prostorová struktura pak dávají proteinům jejich biologické vlastnosti.
Struktura
- aminoskupina (-NH2, volná, substituovaná)
- karboxylová skupina (-COOH)
- další funkční skupiny
Klasifikace
- dle struktury postranního řetězce a funkčních skupin
- dle polarity postranního řetězce
- polární
- nepolární
- dle významu ve výživě člověka
- esenciální = lidský organismus je není schopen vytvořit endogenně
- podmíněně esenciální = esenciální při nepřítomnosti prekurzorů či nezralosti enzymatických systémů
- plně neesenciální
- glycin, alanin, serin, cystein, kyselina asparagová a asparagin, glutamová kyselina a glutamin, selenocystein, tysorin, prolin
| Rozšířená klasifikace | |
|
| Zástupci | |
|
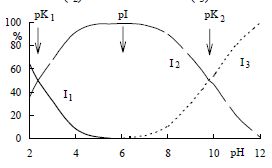
| Fyzikálně-chemické vlastnosti | ||||||||||
|
Význam proteinů pro tělo
Význam proteinů pro lidské tělo je obrovský. Zároveň představují pro tělo jediný zdroj dusíku.
Plní funkce:
- stavební – kolagen, elastin;
- motorické – aktin, myosin;
- informační – proteinové hormony;
- obranné – imunoglobuliny, komplement, antigeny;
- transportní – albumin, umožňují katalýzu (enzymy) a další.