Inzulin
| Inzulin | |
 | |
| Prekurzor | preproinzulin, proinzulin |
|---|---|
| Žláza | endokrinní pankreas |
| Struktura | heterodimer složený ze dvou řetězců (α a β, spojené disulfidovými můstky) |
| Cílový orgán/tkáň | kosterní svalovina, myokard, tuková tkáň, játra |
| Receptor | inzulinový receptor |
| Účinky | zvyšuje vstup glukózy do buněk a proteosyntézu, inhibuje uvolňování glukagonu a tvorbu MK; v játrech: glykogeneze, tvorba TAG, glykolýza, snížená tvorba glukózy a ketolátek; ve svalech: glykogeneze, glykolýza |
| OMIM | 176730 |
Inzulin patří mezi pankreatické hormony. Je produkovaný v specializovaných buňkách pankreatických ostrůvků – tzv. B-buňky. Jedná se o peptidový hormon, reguluje energetický metabolismus. Inzulin je nazýván také hormonem sytosti, nadbytku. Choroby nějakým způsobem spojené s inzulinem (problém v syntéze, problém s buňkami ostrůvků, poruchy receptorů a jejich signalizace) jsou v naší populaci poměrně rozšířené – i laik zná „cukrovku“, tedy diabetes mellitus (DM).
Stavba pankreatického ostrůvku[upravit | editovat zdroj]
B-buňky (60 % z buněk ostrůvků) se nachází převážně v centru, A-buňky (25 %, produkují glukagon), naopak, nejprve na periferii. Arteriola přichází do centra, tam se větví a kapiláry směřují k okrajům myšlené deformované koule. Takto je možné, aby uvolněný inzulin působil na A-buňky, zatímco glukagon se většinou nestihne dostat k B-buňkám (poločas rozpadu 1–3 min, kromě toho je obvykle většina glukagonu vychytaná játry). Toto je dobré si uvědomit, když budeme hovořit o regulaci sekrece hormonů.
Historie[upravit | editovat zdroj]
Inzulin izolovali již v roce 1921 pánové Banting a Best (jako tzv. „ostrůvkový faktor“) z pankreatické tkáně. Patří mu (mezi proteiny) mnohá prvenstva – byl to první protein, u kterého byl podán důkaz hormonální činnosti, první protein, který byl krystalizovaný a sekvenovaný, první uměle syntetizovaný v laboratoři. Na druhé straně – o jeho intracelulárním působení a různých molekulárních mechanizmech víme vcelku málo.
Struktura[upravit | editovat zdroj]
Molekula inzulinu je heterodimer složený ze dvou řetězců (α a β, spojené disulfidovými můstky). V celé molekule jsou tři místa, ve kterých záměna aminokyseliny vyvolá neúčinnost – umístění disulfidových vazeb, hydrofóbní zbytky C-konce β-řetězce a hydrofóbní zbytky obou konců α-řetězce. (Substituce aminokyselin jsou jinak velmi časté, ale pokud k nim dochází mimo zmíněná tři místa, prakticky nemění biologickou účinnost.)
Syntéza[upravit | editovat zdroj]
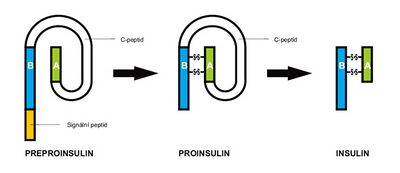
Syntéza inzulinu – tak jako každého proteinu – začíná v jádře transkripcí a pokračuje na ribozomech RER translací – vzniká preproinzulin. Od inzulinu se liší pre- sekvencí (hydrofóbní AMK, slouží jako usměrňovač, t.j. aby molekula cestovala do cisteren RER) a spojujícím C-peptidem (sekvence AMK, která spojuje N-konec α-řetězce a C-konec β-řetezce). Pre- sekvence je odstraněna v RER, vzniká proinzulin. Ten má vhodnou konformaci na to, aby se zoxidovaly -SH skupiny cysteinů a vznikly tak disulfidové můstky mezi α- a β-řetězcem. Následně je proinzulin transportovaný do GA, kde začíná proteolýza (odstranění C-peptidu). Inzulin, malé množství proinzulinu (poměr inzulin/proinzulin je 5:1), C-peptid a minoritní množství dalších látek jsou poté balené do sekrečních granul a po příslušném signálu fúzují s cytoplazmatickou membránou a uvolňují svůj obsah do ECT.
Sekrece inzulinu[upravit | editovat zdroj]
Sekrece probíhá následujícím mechanismem:
- v případě nárůstu hladiny glukózy v plazmě (stav po jídle) – a tedy úměrně i v B-buňkách pankreatu – dojde ke změně membránového potenciálu (depolarizaci);
- depolarizace je způsobena nahromaděním ATP v B-buňkách, které vede k uzávěru ATP-dependentních-K+ kanálů, takže se draslík v buňce hromadí. ATP vzniká v dýchacím řetězci, Acetyl-CoA pro citrátový cyklus prochází z pyruvátdehydrogenázové reakce. Pyruvát vzniká aerobní glykolýzou;
- jelikož začíná metabolismus glukózy v B-buňkách glukokinázou (Km = 10 mmol/l, ten stejný enzym se nachází ještě v hepatocytech), je potřeba, aby hladina glukózy stoupla v plazmě na hodnotu cca 8–10 mmol/l. Tímto mechanismem je zajištěno, aby velké množství ATP vznikalo pouze při vysokých hladinách glukózy (transportér pro Glc SLC2A2 je aktivní při vyšších hladinách, normální hladina Glc je 3,6–5,5 mmol/l);
- v důsledku depolarizace se otevírají Ca2+ kanály, stoupne hladina vápníku v cytoplazmě B-buněk a dojde k fosforylaci cytoskeletu – sekreční granula splývají s membránou (Ca2+ je potřeba jako kofaktor pro kinázy);
- postprandiální sekrece probíhá ve dvou „fázích“ (resp. dva píky na křivce hladiny inzulinu v plazmě v závislosti na času) – ranná a pozdní fáze;
- na myších bylo pozorováno, že sekreci inzulinu zvyšuje také osteokalcin (glykoprotein produkovaný osteoblasty v kosti), stejně jako proliferaci B-buněk. V lidském těle zatím není jasné, co způsobuje komunikaci mezi kostmi a regulací energetického metabolismu. V současnosti je zřejmé, že inaktivace tzv. PTPRV genu (kóduje tyrozinfosfatázu přítomnou v kmenových buňkách, Sertoliho buňkách a osteoblastech) má pozitivní vliv na proliferaci B-buněk a sekreci inzulinu;
- na druhé straně je sekrece inzulinu inhibovaná somatostatinem;
- v klinice je důležité stanovení množství C-peptidu jako markeru endogenní produkce inzulinu. Využívá se k rozlišení cukrovky prvního a druhého typu, zejména u pacientů léčených exogenně podávaným inzulinem.
Mechanismus účinku[upravit | editovat zdroj]
Inzulinový receptor[upravit | editovat zdroj]
Na membráně cílových buněk je receptor – heterotetramer. Podjednotka α je uložena extracelulárně, váže hormon. Podjednotku β tvoří transmembránový protein a jeho intracelulární část vykazuje tyrozinkinázovou aktivitu. Podjednotky jsou kovalentně spojené disulfidovými vazbami v poměru α2-β2.
Převod signálu[upravit | editovat zdroj]
V případě navázání inzulinu dojde k oligomerizaci, shluknou se dva (či více) receptorů k sobě, následně se změní konformace molekul – důsledkem je autofosforylace intracelulárních častí sousedních polovin receptorů. Syntéza receptoru a následná degradace probíhá s poločasem rozpadu do 12 hodin. K převodu signálu slouží adaptorové proteiny – v případě inzulinu IRS-1 (inzulin receptor substrate). O druhém poslovi inzulinu se vedou spory. Celá kaskáda končí fosforylací/defosforylací cílových proteinů, popř. způsobuje vystavení transportních proteinů nebo působí na DNA (viz další odstavec). Dochází taktéž k internalizaci („pohlcení“) komplexu hormon-receptor.
Degradace[upravit | editovat zdroj]
Inzulin je degradovaný (zejména v játrech, z části v ledvinách a placentě) enzymem inzulinázou, popř. glutathion-inzulin-transhydrogenázou (játra), receptor je znovu vystavený na membráně.
Down-regulation[upravit | editovat zdroj]
V případě, že je koncentrace inzulinu vysoká, klesá citlivost tkání na inzulin (tzv. „down-regulation“ – snížení počtu receptorů na membránách). To se podílí na vzniku inzulinové rezistence u DM II.
Působení inzulinu[upravit | editovat zdroj]
Inzulin zvyšuje transport glukózy z krve do buněk kosterní svaloviny, myokardu a tukové tkáně. Děje se tak díky tomu, že hormon způsobí vystavení glukózových transportérů GLUT4 (ty byly zatím připravené v pohotovosti v ICT) na membráně. Děje se tak zejména v buňkách kosterní svaloviny, kardiomyocytech a adipocytech. Různými metodami (subcelulární frakcionace, elektronová a fluorescenční mikroskopie) bylo prokázáno, že v nepřítomnosti inzulinu je v těchto tkáních většina (cca 95 %) množství GLUT4 umístěna intracelulárně.
Jelikož se inzulin vyplavuje po jídle – za hladovění (nebo několik hodin po jídle) klesá jeho hladina – glukóza je během většiny dne (člověk je všeobecně připravený spíše na přežívání nedostatku než nadbytku…) šetřena pro mozek právě díky tomu, že se do svalů a do tuku nedostane, resp. dostane v malém množství (chybí GLUT4 na membráně, protože chybí inzulin).
Účinky na energetický metabolismus[upravit | editovat zdroj]
Jsou odvozeny od stavu, ve kterém se člověk nachází po jídle. Tělo dostalo dávku glukózy, kterou je potřeba zpracovat. Proto bude aktivní glykolýza, glykogeneze, lipogeneze a ukládání lipidů v adipocytech. Samozřejmě, pokud je třeba, glukóza se ihned spotřebuje (např. pracujícím svalem, mozek žije téměř pouze z glukózy…). Inzulin snižuje množství cAMP, resp. inhibuje přeměnu neaktivní adenylátcyklázy na aktivní. Díky tomu:
- nevznikne proteinkináza A (zůstane v inaktivním stavu jako PKB), která by přeměnila aktivní glykogensyntázu na inaktivní glykogensyntázu;
- zůstane inaktivní fosforyláza, která je řídícím enzymem glykogenolýzy;
- na lipogenezi působí aktivací acetyl-CoA-karboxylázy a zároveň nízkou hladinou cAMP inhibuje lipolýzu.
Působením na DNA indukuje inzulin biosyntézu enzymového komplexu syntázy mastných kyselin a snižuje syntézu fosfoenolpyruvátkarboxykinázy (regulační enzym glukoneogeneze). V játrech inhibuje ketogenezi, způsobuje růst buněk.
Je dobré si uvědomit, že na metabolismus jako takový musíme nahlížet jako na velký celek. Jak ovlivníme metabolickou dráhu v nějaké buňce, v jiných buňkách to nezůstane bez odezvy. Proto na jedné straně vidíme přímé působení inzulinu (jednoduše navázáním se na receptor v membráně), na druhé straně nenápadné nepřímé zásahy do děje (např. blokáda lipolýzy v adipocytech způsobí v játrech nedostatek FFA, proto budou játra zpracovávat zejména glukózu).
Kromě toho má inzulin pozitivní vliv na růst a replikaci buněk, na hojení ran (poznámka: v kulturách fibroblastů způsobuje inzulin schopnost růstových faktorů (FGF, PDGF, EGF…) stimulovat buněčný cyklus).
Fetální období[upravit | editovat zdroj]
Inzulin se začíná tvořit v 10. týdnu a působí také na fetální organogenezi (placenta je pro inzulin nepropustná, proto se tam mateřský inzulin nedostane).
Inzulin v terapii[upravit | editovat zdroj]
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
- Inzulinoterapie
- Hormony lidského těla: ADH • Estrogeny • Erytropoetin • Gestageny • Glukagón • Glukokortikoidy • Choriový gonadotropin • Inzulin • Katecholaminy • Kalcitonin • Noradrenalin • Parathormon • Prostaglandiny • Renin-angiotenzin-aldosteronový systém • Růstový hormon • Testosteron
- C-peptid
- Diabetes mellitus
- Hepatogenní diabetes a metabolizmus sacharidů
Externí odkazy[upravit | editovat zdroj]
Použitá literatura[upravit | editovat zdroj]
- DUŠKA, František. Biochemie v souvislostech, 1.díl – základy energetického metabolizmu. 1. vydání. Praha : Karolinum, 2006. ISBN 80-246-1116-3.
- MURRAY, Robert K.. Harperova biochemie. 2. vydání. Jinočany : H&H, 1998. ISBN 80-7319-013-3.
- MOORE, Keith L. a PERSAUD. Zrození člověka: embryologie s klinickým zaměřením. 1. vydání. Praha : ISV, 2002. 564 s. ISBN 80-85866-94-3.
- GUYTON, Arthur C. a John E. HALL. Textbook of medical physiology. 11. vydání. Philadelphia : Elsevier Saunders, 2006. 1116 s. ISBN 0-8089-2317-X.
- LENEY, Sophie E. a Jeremy M. TAVARÉ. The molecular basis of insulin-stimulated glucose uptake: signalling, trafficking and potential drug targets. Journal of Endocrinology. 2009, vol. 72, no. 203, s. 1-2, ISSN 1479-6805.