Portál:Otázky z biofyziky (1. LF UK, VL)/93. Otázka
| 93. Otázka | ||||
| Využití ionizujícího záření v medicíně | ||||
| Otázky z biofyziky (1. LF UK, VL) | ||||
| Předchozí • Další | ||||
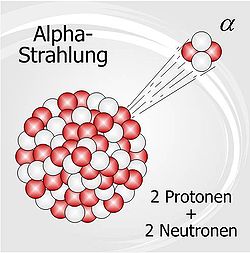
Záření alfa
Záření α je korpuskulární (částicové) záření, jehož částicemi je proud jader helia 4He. Částice α vznikají při α-rozpadu těžkých jader popsaném rovnicí:
Takto vzniklé částice mají jen několik možných hodnot energie; částice α si odnášejí rozdíl energií mezi mateřským a dceřiným jádrem. Říkáme, že α-záření má čárové energetické spektrum, to znamená, že energie uvolněných α-částic může nabývat jen určitých, pro daný druh jádra specifických hodnot.
Interakce záření α
Částice α má poměrně velkou hmotnost a nese 2 kladné elementární náboje. Ionizační ztráty při průchodu absorbátorem jsou značné. Zhruba polovina energie se ztrácí ionizací a druhá polovina důsledkem excitace. I když může být rychlost vzniklých α-částic velká, jejich dosah na vzduchu je jen krátký. Záření lze odstínit i listem papíru. Nebezpečná je především vnitřní kontaminace, tedy vpravení α-zářiče do organismu. Může docházet k uvolnění velkého množství energie malému objemu tkáně, což má negativní biologický účinek.
Využití v medicíně
Záření alfa se v medicíně často užívá k terapii. Především pak v oftalmologii, kdy se zářič implantuje do oka. To je tzv. brachyterapie.
Odkazy
Související články
Záření β
Záření beta má v medicíně využití především v diagnostických metodách. Záření β+ je používáno v pozitronové emisní tomografii. Zatímco záření β- hraje významnou roli ve výrobě RTG záření.
Zářenní γ
Gama záření je v medicíně využito v řadě diagnostických a radioterapeutických metod, mezi něž patří:
Gama nůž
Leksellův gama nůž (LGN) je integrovaný systém, který se využíva v stereotaktické radiochirurgii. Je založen na fokusovaném gama záření z velkého počtu radioaktivních zdrojů. Je registrovanou obchodní známkou švédské firmy Elekta Instruments AB. V současnosti je dostupných pět modelů LGN − model U (původní), model B, model C, model 4C a Perfexion.
Fyzikální principy
V LGN se využívají fotony, které vznikají při radioaktivní přeměně radionuklidu Co60 na Ni60. Energie fotonů je vysoká − střední energie je 1,25 MeV. Protože fotony nejsou nositelem náboje, dochází v monoenergetickém svazku k exponenciálnímu snížení počtu fotonů s rostoucí hloubkou průniku do daného materiálu. Tedy dávka směrem od povrchu nejprve narůsta do své maximální hodnoty, která je pro danou energii fotonového svazku charakterizována určitou hloubkou. Poté dávka s rostoucí hloubkou exponenciálně klesá.
Z uvedeného odstavce vyplývá, že průběh svazku je pro stereotaktickou radiochirurgii nevýhodný a proto je nutné použít velkého počtu kolimovaných izocentrických svazků, které se protínají v jediném bodě, izocentru. Bodem se rozumí objem s vysokou koncentrací dávky, a jeho velikost se přibližně rovná velikostí použitého kolimátoru. Tímhle způsobem docílíme maximální absorbovanou dávku za současného prudkého spádu dávky do okolí.
Komponenty
Leksellův gama nůž tvoří tři hlavní komponenty:
- radiační jednotka se čtyřmi kolimačními helmicemi a léčebným lůžkem;
- Leksellovo stereotaktické instrumentárium;
- plánovací systém tzv. Leksellův GammaPlan.
V radiační jednotce se využívá 201 zdrojů Co60, které jsou umístěny fixně v hemisférické centrální jednotce o poloměru 400 mm. Zdroje nejsou umístěny libovolně ale v pěti řadách po obvodu jednotky.
V každém zdroji se nachází 12−20 válcových pelet o průměru a délce 1 mm, které jsou uzavřeny ve dvou pouzdrech z nerezové oceli. Pouzdra jsou pak umístěna do hliníkového držáku. Veškeré záření je usměrňováno (kolimováno) třemi kolimátory − dva nacházíme v radiační jednotce a jeden je ve výměnné kolimační helmici. Kolimační helmice v ozařovací poloze vytváří kolimační otvory (celkem 201) tvořící kanály jejichž osa směřuje do ohniska v centru radiační jednotky s přesností 0,3 mm. Kolimační kanál je dlouhý 217,5 mm a může být nahrazen zátkou, která odstíní daný svazek. To se využívá k zaslepení takového svazku záření, který by procházel kritickou strukturou, nebo při zaslepení více kolimátorů s cílem dosáhnout ideální prostorové dávkové distribuce.
Jako stereotaktické instrumentárium je používaný stereotaktický rám, který je fixován k hlavě pacienta pomocí čtyř šroubů, které se pevně připojí do lebeční kosti. Šrouby jsou vyrobené z hliníku a zakončené titanovými hroty. Stereotaktický rám je vyroben z nemagnetických slitin hliníku a titanu.
Plánovací systém Leksell GammaPlan je provozován na počítači s operačním systémem LINUX. Data jsou uchovávána v databázi a přes hesla jsou přístupná co umožňuje konzultaci s jiným pracovištěm.
Pro práci s LGN není nutná speciální ozařovna protože nedochází k výstupu žádného primárního svazku mimo stínící těleso.
Postup při přijetí pacienta
- Po nálezu nitrolebního onemocnění, které by bylo vhodné léčit gama nožem, následuje krátká hospitalizace.
- Po přijetí je pacient o fungování a léčbě gama nožem instruován lékařem.
- Večer a ráno před ozářením si pacient umyje vlasy desinfekčním alkoholovým roztokem.
- Na noc a ráno dostane uklidňující léky.
- Před výkonem je nutné si sundat všechny kovové předměty.
- Na hlavě se provede lokální znecitlivění a po propíchnutí kůže se čtyřmi hroty připevní stereotaktický rám. (podrobněji viz oddíl Proces léčby)
- Pacient je vyšetřen rentgenovou nebo magnetickou resonancí.
- Poté se několik hodin připravuje ozařovací plán, zatímco pacient odpočívá → Řídící počítač celého systému kontroluje všechny parametry důležité ke správnému ozáření pacienta (velikost kolimátoru, počet isocenter, ozařovací čas, stereotaktické souřadnice).
- Pacient je poté položen na lůžko ozařovacího přístroje a pomocí mikrofonu a reproduktoru komunikuje s personálem.
- Samotné ozařování trvá několik minut. Může se však opakovat.
- Poté se pacientovi sejme stereotaktický přístroj a je odeslán k odpočinku.
- Případná nevolnost či bolest hlavy do druhého dne odezní.
Proces léčby
- etapa − získání diagnostických snímků s vyznačenou lokalizací léčené léze pomocí zobrazovacích metod, jako je výpočetní tomografie (CT), nukleární magnetická rezonance (MR), angiografie (AG) případně pozitrónová emisní tomografie (PET).
- etapa − stanovení dávkového rozložení v lézi a jejím okolí, prováděno ve výpočetní matrici.
- etapa − stanovení rozměrů hlavy pomocí kulové helmice z plastu, které má střed geometricky totožný se stereotaktickým rámem. Umísťuje se na základnu rámu a pomocí měřítka se proměří vzdálenost od lebky k povrchu plastikové helmice a taky se stanoví tloušťka tkáně od středu rámu k povrchu hlavy.
- etapa − začíná vlastní léčebný proces, a to nasazením stereotaktického rámu na hlavu pacienta, v lokální anestezii. Rám musí být dostatečně fixován aby nedošlo k posunutí. Rám nelze používat u pacientů do věku 2 let kvůli nedostatečné osifikaci a rigiditě kalvy.
Po inicializaci léčby se stínící dveře na radiační jednotce otevřou a pacient ležící na lůžku zajede do radiační jednotky. Tady se zakryjí primární stacionární kolimátory s výměnnými kolimátory v helmici. Správnost polohy je kontrolovaná mikrospínačem s přesností na 0,1 mm. Až uplyne časový interval na ozařování, který byl stanoven ozařovacím plánem, tak se lůžko vrátí do výchozí polohy a stínící dveře se následně uzavřou. Aby se pokryl celý objem cílového ložiska může být zapotřebí větší množství takových zásahů, v závislosti na velikosti a tvaru ložiska. Obvykle je jejich počet menší než 15 a zpravidla nepřevyšuje 30.
Indikace
Obecně se LGN užívá na procesy, jejichž hranici lze snadno definovat (není např. vhodný na glioblastomy):
- Kavernózní malformace – indikace a komplikace identické s AVM, rozdíl je pouze v tom, že rebleeding je u kavernomů častější, ve valné většině se ale jedná o klinicky méně signifikantní krvácení.
- Vestibulární schwannom – ozařujeme hlavně menší nádory, výhodou je možnost zachování sluchu (pokud již nebyl poškozen) a vyloučení poškození lícního nervu.
- Neurinomy ozářením nezmizí, část se jich zmenší (44 %), část neroste (42 %), část pokračuje v růstu.
- S odstupem může dojít k projevům postižení hlavových nervů (n. V,VII,VIII).
- Meningeomy – hlavně špatně přístupné na bazi, u menších, při kontraindikaci operace u pacientů v těžkém stavu.
- Metastázy – v jednom sezení je možné postupně ozářit i několik metastáz (lze je dobře centrovat).
- Adenom hypofýzy – musí být aspoň 5 mm od n. II, aby nedošlo k poškození zraku.
Komplikace po ozáření
V souvislosti s gama nožem se setkáváme s poradiačními změnami, které jsou buď akutní nebo pozdní.
- Akutní − vznikly od dne ozáření do 90 dnů po léčbě, přičemž závažnost časných změn nemusí odpovídat závažnosti změn pozdních. Například při ozáření v blízkosti IV. mozkové komory se může objevit nauzea a zvracení, obvykle ustoupí do 48 hodin.
- Pozdní − komplikace, které vznikly 90 dní po ozáření, doporučený časový interval pro sledování pozdních komplikací je 5 let. Pozdní komplikace se objevují především ve tkáních a orgánech složených z diferencovaných buněk s minimální schopností obnovovat své buňky. Tak dojde ke ztrátě funkce části nebo celého orgánu. U rychle se obnovujících tkání (například sliznice) dochází k výměně buněk během hodin a dnů.
Výhody léčby LGN
- Minimálně invazivní metoda;
- nezasahuje zdravou tkáň;
- pro práci s LGN není nutná speciální ozařovna protože nedochází k výstupu žádného primárního svazku mimo stínící těleso;
- bez celkové anestezie;
- rychlý čas rekonvalescence;
- úspěšnost léčby okolo 90 %.
SPECT
Jednofotonová emisní výpočetní tomografie (Single-Photon Emission Computed Tomography, SPECT, někdy také tomografická scintigrafie) je diagnostická zobrazovací metoda používaná v nukleární medicíně. Využívá scintilačních kamer k rekonstrukci obrazu rozložení radiofarmaka v těle pacienta.
Princip
Principem je podání radiofarmaka s γ zářením (nejčastěji 99mTc) a pořízení řady scintigrafických snímků pacienta z několika směrů v rovině tomografického řezu. Používá se nejčastěji jedné až několika scintilačních kamer, které se otáčí kolem vyšetřovaného po malých úhlových krocích. Rozložení radiofarmaka v tomografickém řezu je pak matematicky rekonstruováno z jednotlivých snímků za využití metody zpětné filtrované projekce, anebo stále častěji metody iterativní algebraické rekonstrukce.
Transmisní SPECT se používá jako analogie CT, kdy je zabudován do přístroje radiozářič o známé aktivitě a jiné energii, než je zářič v těle pacienta. Využívá se pro korekci chyby v kvantifikaci záření.
Moderní přístroje nahrazující transmisní SPECT fungují jako hybridy, kdy je zabudované SPECT a tzv. low-dose CT v jednom. Umožňují tak sledovat anatomickou i funkční strukturu tkáně.
Zachycení záření
Kolem dlouhé osy pacienta rotují jedna až tři gamakamery, které tak mohou záření snímat z různých úhlů a tvořit tak transverzální, frontální i sagitální řezy tělem pacienta, a tak vytvořit 3D zobrazení patologického ložiska.
Detekční hlava gamakamery
Až několik centimetrů vysoká olověná deska nacházející se těsně před krystalem se souběžnými průchody (až několika tisíci) kolmými ke krystalu. Kolimátor propouští ke krystalu jen ty fotony, které k němu přichází v kolmém směru, a tím tlumí šum a zajišťuje větší přesnost výsledného obrazu.
- Krystal
V krystalu probíhá scintilace fotonu. Krystal bývá zhotoven z jodidu sodného (NaI) a je kruhovitý či obdélníkovitý, v průměru dosahuje 40−50 cm a jeho tloušťka je kolem 1 cm. Plocha krystalu odpovídá ploše registru záření.
- Fotonásobiče
Pro vyšší přesnost se používá i více než 90 fotonásobičů. Každý fotonásobič zaregistruje, že v krystalu došlo ke scintilaci fotonu − ten, na který dopadne záření nejvíce, naměří nejvyšší hodnoty a naopak fotonásobiče, které jsou od místa dopadu dál, naměří méně. Naměřené hodnoty se převedou na elektrické signály. Pro větší přesnost se vyberou pouze dva nejsilnější signály (jeden pro souřadnici x a druhý pro souřadnici y na ploše krystalu), které odpovídají poloze absorpce fotonu, a ty se vyšlou dále do osciloskopu.
Osciloskop
Díky horizontálním a vertikálním vychylovacím destičkám se elektronový paprsek vychýlí na stínítko a tím se na stínítku zobrazí světelný bod v místě, které odpovídá poloze scintilace fotonu v krystalu.
→ Celý systém je pokrytý olověnou vrstvou, která zabraňuje působení vnějších podmínek na proces přenosu informace o poloze scintilace fotonu v krystalu.
Počítač
K přístroji bývá trvale připojený jednoúčelový počítač, do jehož paměti se ukládají výsledná zobrazení.
Světelný bod na stínítku zachytíme do elektronické paměti počítače.
Gamakamera se nechá zapnutá tak dlouho, dokud se nezobrazí celý požadovaný obraz.
V paměti počítače si lékař může prohlížet jednotlivé série zobrazení.
Díky speciálním programům umí počítač analyzovat celou studii a vypočíst příslušné údaje.
Počítač také seskládáním řezů vytvoří 3D zobrazení daného patologického ložiska. K tomu využívá přednastavených matematických algoritmů, např. filtrované zpětné projekce, která pro přesnější zobrazení zesiluje informaci ze stínítka a potlačuje šum.
Využití
SPECT se využívá např. v kardiologii, neurologii či onkologii. Zobrazuje funkci orgánu či metabolickou aktivitu části těla (stejně jako PET), nikoli jeho anatomické struktury (MRI, CT).
- Kardiologie
V kardiologii se vyšetřuje srdeční sval − myokardiální perfuze (ischemická choroba srdeční), metabolismus myokardu. Jde o dvojí vyšetření − před a po zátěži. Také se dají vyšetřit plíce nebo žilní systém.
- Neurologie
V neurologii se zjišťuje prokrvení mozku. Díky vyšetření se dá lokalizovat postižené místo a diagnostikovat tak nemoc (demence, Alzheimerova choroba, Parkinsonova choroba), nebo i najít místo, kde přesně má proběhnout operace mozku (epilepsie − dvojí vyšetření − před a při záchvatu).
- Onkologie
SPECT pomáhá při lokalizaci nádorů. Využívá se při lymfoscintigrafii, vyšetření sentinelových uzlin apod.
- Jiné změny metabolismu
Lokalizace zánětů, úrazů, onemocnění kloubů či hojících se ložisek.
Výhody a nevýhody
Výhodou oproti planární scintigrafii je vyšší kontrast snímků a především možnost kvantifikace radiofarmaka ve tkáni. Samotná SPECT představuje menší radiační zátěž pro pacienta než CT.
Nevýhodou jsou někdy až velmi nepřesné výsledky kvantifikace vlivem atenuovaného (oslabeného) záření, které vzniká Comptonovým nebo fotoelektrickým jevem. Radiační zátěž jednoho vyšetření závisí nejvíce na aktivitě a efektivním poločasu (rozpadový a biologický poločas) použitého radiofarmaka. Další nevýhodou je dlouhá doba vyšetření.
PET
Pozitronová emisní tomografie (Positron Emission Tomography, PET) je diagnostická zobrazovací metoda umožňující na tomografických řezech sledovat rozložení radiofarmaka v těle pacienta. Je používána zejména v neurologii, kardiologii a onkologii.
Princip vyšetření přístrojem
Pacientovi je podán β+ zářič s velmi krátkým poločasem, nejvýše desítky minut. Rozpadající se radiofarmakum produkuje pozitrony, které prakticky ihned anihilují s elektrony (pozitron je antičástice elektronu) za vzniku dvou fotonů záření gama. Vzniklé fotony odlétají v právě opačném směru se stejnou energií 511 keV.[1] Toho, že vzniklé fotony odlétají vlastně po přímce, se využívá při detekci. Detekovaný je pouze takový foton, ke kterému byl na detekčním prstenci zachycen i jeho protějšek, hovoříme o koincidenčním zapojení. Výsledný tomografický obraz je pak dán zpracováním velkého množství takto zachycených párů.
V zásadě se používají dva druhy stavby detektorů v přístroji:[1]
- sudý počet detektorů rotujících kolem pacientova těla;
- několik set až tisíce pevných detektorů uspořádaných v přístroji v několika prstencích. Protilehlé detektory ve stejném prstenci jsou spojeny tak, aby mohly registrovat pouze takové páry fotonů, které s nimi interagují ve stejném čase.
Detektory nejsou scintilátory s běžnými krystaly kvůli vysoké energii fotonů, proto se používají scintilátory s krystaly o větší hustotě a s vyšším atomovým číslem. Příkladem je např. germaniová sůl bismutu a fluorid barnatý.[2]
Trojrozměrné rekonstrukce obrazů se provádějí v síti procesorů, tzv. transputerech[1].
Pozitrony mají ve tkáních dosah asi 2 mm, poté dochází k anihilaci. Jedná se tedy o metodu s velmi vysokou přesností. [3]
Použité zářiče
Obvyklým zářičem je izotop 18F s poločasem 110 minut přeměňující se na kyslík. Podává se nejčastěji ve formě [18F]-fluordeoxyglukózy (FDG), která se přeměňuje na glukózu. Protože se flourdeoxyglukóza chová podobně jako glukóza, je více vychytávána v místech s aktivnějším metabolizmem (např. nádorové buňky). Jiným zářičem s 18F je např. syntetický analog leucinu [18F]-fluciklovin![]() , který se používá pro diagnostiku karcinomu prostaty.
, který se používá pro diagnostiku karcinomu prostaty.
Dalšími zářiči jsou například 11C, 13N, 15O, což jsou biologicky významné prvky. K výrobě takových zářičů s velmi krátkým poločasem rozpadu slouží přímo na místě lékařský cyklotron.
Průběh
Pacient obdrží radiofarmaka injekčně nebo vdechnutím. V případě FDG-PET-vyšetření je použito podle váhy pacienta a typu přístroje (2D a 3D skener) 150 až 700 MBq. Po obdržení se musí počkat 50 až 75 minut, aby radiofarmaka měla čas se nashromáždit na relevantních částech těla. Během vyšetření by měl být zajištěn klid a dostatek tepla. Jinak by se mohlo stát, že tělo pacienta pod vlivem chladu zvýší metabolismus cukru, který je možno vidět ve svalech nebo hnědém tuku.
Při vyšetření je pacient položen na pohyblivý stůl tak, aby zkoumaná část těla byla v dosahu detektorů. Axiální vizuální oblast detektorů je přibližně 15−20 cm. Pro snímek přesahující tuto hranici je zapotřebí různých lůžkových pozic. Doba jednotlivých záznamů je ovlivněna typem přístroje, druhem a dávkou radiofarmak a váhou vyšetřeného. Po dvou až čtyřech minutách přístroj automaticky zaujímá další pozici.
Hybridy
PET je sám o sobě vysoce citlivý proces. Nevýhodou je, že je anatomicky těžké určit místa metabolicky aktivnější, protože v první řadě metabolické procesy určuje. K tomu se ještě započítá omezené místní rozlišení 4−6 mm.
K tomuto účelu byl sestaven přístrojový hybrid používající PET a CT. Kombinací vysokého rozlišení (až k 0,35 mm) a detailním anatomickým znázorněním CT s vysoce sensitivními informace metabolismu s PET se dosahuje kvalitnějších a přesnějších výsledků. Další výhodou je velké zkrácení času pro celkový průběh.
Další možnost je kombinace PET s MR. Výhoda integrace obou v jednom přístroji je synchronní vyšetření pro neurologické a kardiologické potřeby.
Výhody a nevýhody
Jednoznačnou výhodou přístroje je jeho velká diagnostická přesnost a prostorová rozlišovací schopnost. Moderní přístroje mají vyšší detekční účinnost než SPECT, zejména také kvůli absenci užití kolimátorů. Další výhodou je využití biogenních prvků ve sledování metabolismu, které jsou v tomto metabolismu normálně zastoupeny.
Významnou nevýhodou je technická náročnost PET a s tím i pořizovací cena přístroje. Navíc často nezbytné pořízení cyklotronu je také nákladné.
Rentgenové záření
Jeho využití v medicíně spočívá v především v diagnostice, ale i v terapii.
Princip zobrazení pomocí RTG záření
Obecná charakteristika
RTG metody jsou prakticky nejvýznamnější v diagnostické medicíně díky tomu, že jsou nejrozšířenější a nejlacinější. Od času objevení RTG (X-paprsků) W. C. Röntgenem v roce 1895 se neustále zdokonalovali až po dnešní kombinované využití účinků RTG záření a moderních počítačových detekčních a zobrazovacích metod.
Jejich principem je rozdílná absorpce a rozptyl RTG záření v jednotlivých tkáních těla. RTG záření je elektromagnetické vlnění podobné světlu, ale s vlnovou délkou 100 000× menší. Zatímco viditelné světlo má vlnovou délku od 400–760 nm, tak RTG paprsky mají vlnovou délku cca 0,05 nm. RTG záření je ionizující, zdraví škodlivé, na rozdíl od světla viditelného. Proto je potřeba se před RTG zářením chránit (olověné zástěry, zkrácení expozice, dozimetrie).
Podstata vzniku RTG záření
RTG paprsky vznikají v rentgenové lampě složené z kladně nabité anody a záporně nabité katody. Katoda je obyčejně z wolframu a je žhavena stejnosměrným elektrickým proudem o proudu odpovídajícímu 2–3 A a vysílá záporně nabité elektrony. Mezi katodu a anodu se připojuje stejnosměrné napětí až 150 000 V. Mezi oběma elektrodami se vytváří silné elektrické pole, díky němuž se elektrony pohybují velkou rychlostí a narážejí do anody, která je zabrzdí a z jejich kinetické energie vzniká velké množství tepla (99 %) a jen asi 1 % RTG paprsků. Vycházejí otvorem z lampy směrem k pacientovi. RTG záření může být tzv. charakteristické (závisí na materiálu anody) a záření brzdné.
Podstatou vzniku charakteristického RTG záření je to, že elektrony v anodě vyrážejí jiné elektrony z obalů atomů. Elektrony z vyšších hladin zaujímají jejich místo a energetický rozdíl se vyzáří jako RTG záření.
RTG záření je buď tvrdé, s kratšími vlnovými délkami, dobře procházející tkáněmi, nebo tzv. měkké, s většími vlnovými délkami, méně prostupné tkáněmi. Platí, že čím větší je anodový proud, tím tvrdší RTG paprsky vznikají. Též platí, že čím je větší katodový proud, tím je RTG záření intenzívnější.
Tvorba RTG obrazu
RTG paprsky z rentgenové lampy procházejí tělem pacienta, přičemž narážejí na tkáně. Vznikají fotoelektrony (fotoefekt, Comptonův rozptyl a tvorba elektron-pozitronových párů) a ty umožňují vznik obrazu tkání. Fotony RTG záření procházejí přes stěnu lampy, potom jsou nízkoenergetické fotony absorbované v primární cloně (hliník) a po průchodu orgánem jsou absorbované v tzv. Buckyho cloně (tenké olověné pásy), uložené těsně před filmem. Tkáně jako jsou sval a tukové tkáně se znázorňují velice špatně, naopak kostní tkáň ale i vzduchová bublina, např. v žaludku, se zobrazí velmi kontrastně. Proto měkké tkáně jako jícen, střevo, žlučník, vidíme na RTG snímku špatně. Pokud je chceme zviditelnit, podáváme do těla RTG kontrastní látky. Mezi ně patří například baryt (tzv. pozitivní kontrast) nebo jodové kontrastní látky, které užíváme při vyšetření štítné žlázy. Kontrastní látkou ale může být i vzduch, případně kyslík nebo helium. Právě helium používáme při zobrazení mozkových komor pomocí tzv. negativního kontrastu.
RTG obraz je stínový obraz určitého orgánu, přičemž černo-bílý kontrast obrazu velmi závisí na odstupňované absorpci RTG záření tkání. To má za následek odstupňované zčernání RTG filmu. Kromě toho RTG obraz závisí také na charakteru a tloušťce tkáně a také na její tvrdosti či měkkosti RTG záření. V neposlední řadě je obraz znatelně ovlivněn fotografickou emulzí a kvalitou a zpracováním filmu.
Roční dávka RTG záření je max. 5 mSv pro chronické - rakovinné účinky a 50 mSv pro akutní - orgánové účinky.
Skiaskopie
Skiaskopie je diagnostická a intervenční radiologická metoda, která používá dynamického zobrazení RTG obrazu (např. pro zobrazení peristaltiky jícnu, žaludku, střev, pozorování dýchacích pohybů nebo pulzace srdce). Pro snížení radiační zátěže se používá pulzní režim, kdy se obraz vytváří např. 4-krát za vteřinu (nikoliv kontinuálně) a nízké hodnoty mAs s automatickým řízením kermového příkonu.
Typy vyšetření
Monokontrastní – Použití pouze pozitivní kontrastní látky (u dětí se používá především tato metoda).
Dvojkontrastní – Použití pozitivní a negativní kontrastní látky.
U žen ve fertilním věku je snaha dodržovat tzv. pravidlo 10 dnů. Vyšetření se provádí během prvních 10 dnů menstruačního cyklu, nakolik dochází k aplikaci vyšších dávek záření na břišní oblast.
Typy kontrastních látek
Negativní – vzduch (irrigografie), metylcelulóza (enteroklýza).
Pozitivní – baryová suspenze, jodové kontrastní látky.
Skiaskopické metody
Mezi skiaskopické metody se řadí:
- RTG vyšetření trávícího traktu: RTG jícnu, videofluoroskopie, RTG žaludku, RTG pasáž, enteroklýza, irigografie, defekografie, zavedení stentů pod RTG kontrolou.
- Vyšetření a intervence močových cest: ureterocystografie, zavedení pig-tail katetru.
- Fistulografie: nástřik ústí píštěle či drénu kontrastní látkou.
- Skiaskopie bránice: diagnostika parézy bránice.
- Skiaskopie plic: odlišení uzlu v plicním parenchymu od extraparenchymových lézí či sumací.
- Cholangiografie: peroperační, T-drénem, PTC (perkutánní transhepatická cholangiografie), ERCP.

|
RTG jícnu: tumorózní stenóza |
| Cholangiografie T-drénem: choledocholithiáza |
Skiagrafie
Skiagrafie je diagnostická metoda pro zobrazení tvrdých i měkkých tkání, která využívá rentgenové záření. Funguje na principu odlišné hodnoty pohlcení procházejícího svazku RTG záření v různých tkáních. Výsledný obraz je zachytáván na citlivý materiál – rentgenový film či detekční systém přístroje (tímto se právě metoda odlišuje od skiaskopie, kde je daný obraz pouze pozorován, avšak není zachycen na záznamové médium). Z obrazu poté můžeme odhadnout vnitřní stavbu či poranění vyšetřovaného orgánu nebo struktury. Nejčastěji se tato metoda používá k vyšetření kostí, zubů a kloubů, ale lze jí zobrazit i měkké tkáně jako jsou např. svaly či plíce. Je to jedna z prvních diagnostických metod u většiny onemocnění.
Technika snímkování
Při většině snímkování se dělají dvě projekce z důvodu dvojrozměrnosti obrazu – předozadní (anteroposterior) a boční. Díky tomu je možné zjistit prostorové uložení zobrazených struktur. Výjimkou jsou snímky hrudníku, které se dělají zadopředně (posteroanterior). Důležité je přitom označit snímky písmeny L nebo P (v závislosti na levé/pravé straně) a signofotem, který obsahuje základní údaje o pacientovi. Rentgenové paprsky pronikají lidským tělem. Při jejich průchodu dochází k různému stupni zeslabení (pohlcení záření), což nám dovolí zobrazit tkáně na speciální RTG filmy. Vzniklý obraz je negativ, na kterém lze rozpoznat jednotlivé struktury těla projasněním a zastíněním. Jasnější místa představují struktury absorbující více záření, zato tmavá místa jsou struktury, kde je absorbováno záření méně. K vyhodnocení snímků se používá přístroj zvaný negatoskop. Využívá se tvrdých technik, kdy je snímkování pořizováno při napětí rentgenky nad 100 kV (např. pro snímkování plic, tvrdých tkání) a měkkých technik při napětí do 45 kV (např. snímkování prsu). Pro snížení radiační zátěže obsluhy i pacientů je nutné používat filtrování a clonění RTG svazku. Primární filtr (clona) slouží k pohlcování nízkoenergetických fotonů a umisťuje se v blízkosti rentgenky. Sekundární filtry (Lysholmova clona s nepohyblivou mřížkou pro snímkování za nepříznivých podmínek - na lůžku nebo operačním sále nebo lépe Buckyho clona, která se nepravidelně pohybuje a tudíž nevrhá ostrý stín na výsledný snímek) se umisťují mezi pacienta a filmovou kazetu, kde funguje jako past na rozptýlené fotony.
- Metoda přímé digitalizace (DR) – expozice detekována přímo ve speciálním detektoru, jenž je součástí přístroje; okamžitá generace obrazové informace.
- Metoda nepřímé digitalizace (CR) – obrazová dokumentace se získává,,čtením“ (digitalizací informace z folie ve speciálním digitizéru).
Aby se dosáhlo většího kontrastu a citlivost metody, používá se ke snímkování speciální RTG filmy s výrazně silnější emulzní vrstvou a vyšším podílem halogenidů stříbra.
Kontrastní látka
Vyšetření lze snáz provést s použitím kontrastní látky, která umožní dokonalé zobrazení tkání. Látka dokáže měnit velikost absorpce záření v těle, a tím vyvolává v rentgenovém obraze větší rozdíly v transparenci vyšetřované tkáně či orgánu oproti okolí. Může být pozitivní nebo negativní. Mezi pozitivní kontrastní látky patří např. jodové či baryové. Mezi negativní vzduch, kyslík či CO2. Před jejím použitím je však nutné prodiskutovat s pacientem možné alergické reakce, a tím vyloučit nežádoucí účinky kontrastní látky.
Negativní kontrastní látky
Tyto látky pohlcují záření méně něž vyšetřovaný orgán. Negativní kontrastní látky se tak využívají pro projasnění rentgenových snímků. Mezi tyto látky se řadí např. vzduch, oxid uhličitý, oxid dusný (rajský plyn).
Pozitivní kontrastní látky
Látky s vysokým protonovým číslem, které mají vysokou absorpční schopnost a na snímcích dávají sytý stín. Pozitivní kontrastní látky se dělí do dvou skupin a to na jodové a baryové kontrastní látky. Jodové kontrastní látky mají nejčastěji tekutou formu (jodové organické sloučeniny ve vodě) a využívají se při lymfografii. Baryové kontrastní látky obsahují síran barnatý a používají se pro vyšetření trávicího traktu.
- Metoda dvojího kontrastu: Při vyšetřování trávicího traktu se někdy používají současně negativní i pozitivní kontrastní látky.
Kontraindikace
Relativní u těhotenství, zejména v prvních čtyřech měsících. RTG záření by totiž mohlo poškodit plod.
Klasické snímkování
U této metody se místo štítu využívá rentgenového filmu, na kterém po expozici zářením vzniká latentní obraz. Tento obraz je dvojrozměrný záznam trojrozměrného objektu. Nejčastěji se využívá fóliových filmů s fotografickou emulzí, které jsou uloženy mezi zesilovacími fóliemi. RTG záření dopadající na tuto fólii vyvolává fluorescenci a významně zesiluje účinek záření na film. Film se následně vyvolá stejným postupem jako ve fotografické praxi. Vzniklý obraz je negativem, na kterém se projevují struktury těla projasněním a zastíněním. Struktury absorbující více záření vytvářejí jasnější místa, struktury absorbující méně záření vytvářejí tmavší místa (díky negativu). Vyhodnocení snímků se děje nejčastěji pomocí negatoskopu – lékařského přístroje, který vydává homogenní intenzivní světlo.
Digitální snímkování
Modernější metoda, kdy se snímky získávají v digitální podobě. Děje se tak několika způsoby:
- Výpočetní radiografie – využití fosforových fólií, které jsou umístěny v podobných kazetách jako RTG filmy. Obraz je získán skenováním kazet laserem po jednotlivých bodech, a je tak přenesen do počítače.
- Přímá radiografie – záření je zachyceno maticí detektorů, kde je převedeno rovnou na elektrický signál. Výhodou této metody je vysoká kvalita obrazů, možnost úpravy obrazu v počítači (jas, kontrast atd.), archivace snímků v digitální podobě a snadná distribuce po nemocnici nebo mimo ni. V neposlední řadě také nižší ekonomické náklady. Nevýhodou je vyšší pořizovací cena zařízení.
Výhody
Rentgenové snímky jsou trvalým dokladem. Vysoká rozlišovací schopnost fotografického materiálu umožňuje studium i velmi malých podrobností.
Nevýhody
Snímky nedokážou zachytit celý děj, ale pouze jeho výsek, a proto nemohou sloužit k přesnému studiu funkce orgánů lidského těla. Metoda neumožňuje ani zachytit prostorovou představu při lokalizování chorobného ložiska tak, jako to jde metodou skiaskopie. RTG vyšetření má ionizační účinky na lidský organismus, které přináší jistá rizika.
Výpočetní tomografie a Hounsfieldovy jednotky
Výpočetní tomografie [pozn. 1](také Computed Tomography, CT, či výpočetní tomografie) je jedním z nejpodstatnějších objevů rentgenové diagnostiky. Je to vlastně matematická rekonstrukce obrazu získaná z řady rentgenových projekcí provedených v různých úhlech. S její pomocí můžeme neagresivním způsobem zobrazit měkké tkáně jako například mozek, slezinu, pankreas, ledviny či svalstvo. Zjistit však můžeme pouze patologické procesy lišící se svou denzitou od okolí. Často je také pacientovi podána kontrastní látka pro lepší rozlišení patologické tkáně.
Historie a generace CT
Teorii rekonstrukce tomografického řezu z mnoha sumačních snímků vypracoval americký fyzik Allan Cormack již v roce 1963, ovšem s využitím záření gama. První použitelný tomograf, EMI mark I, však sestrojil až angličan Godfrey Newbold Hounsfield v roce 1972. V roce 1979 byla Cormackovi i Housfieldovi udělena za objev výpočetní tomografie Nobelova cena.
Z hlediska konstrukce systému zdroj záření/systém detektorů je možné rozdělit přístroje do několika generací. Známe šest systémů generace CT, z nichž se dnes používají systémy třetí až šesté generace.
- generace: Houndsfieldův systém, který se po pootočení o 10°–15° posunul lineárně přes celou šířku pacienta v dané rovině. (rekonstrukce do 5 minut),
- generace: Využívá také rotačně translační pohyb, menší úhel mezi jednotlivými snímky (3°–15°) a vetší počet detektorů (6–60). (rekonstrukce 10s–20s),
- generace: Tato generace je dnes nejužívanější. Pracuje za rotace rentgenky o 360°, se širokým snopcem záření a za použití mnoha detektorů (400–600) na protilehlé matici. Snímkování je prováděno po 1° až 0,5°. Záznam se snímá po celou dobu plynulé otočky, za pulzní obsluhy rentgenky. Doba skenu do 1 sekundy. Spirální (helikální) CT, je pokračováním přístrojů 3. generace. První systém CT s kontinuální rotací byl vyvinut firmou Bio-Imaging Research v roce 1986. Dříve bylo nutné každou následujíc otočku provádět v opačném směru než tu předchozí, mezitím se stůl s pacientem posunul. Zavedení kontinuální rotace umožnilo plynulý posun stolu s pacientem, zatímco se kontinuálně zaznamenávají snímky. Tato metoda umožnila lepší vytváření 3D rekonstrukcí a urychlila celý proces získání snímků. Helikální CT se uplatňuje především v CT angiologii.,
- generace: Využívá rotačně-stacionární systém: Široký svazek, tisíce stacionárních detektorů v kruhu. Rotuje pouze rentgenka, o 360°. Problém vzniká při expozici okrajových detektorů, které jsou zasaženy rozptýleným zářením. Tento systém je však náročný a v praxi se příliš nerozšířil.
- generace: Jde o systém nutační, který se skládá z matice fixních detektorů a rotující rentgenky. Podle její polohy se detektory vychylují z kolmice tak, aby na ně paprsky dopadly kolmo. Zpracování obrazu nabízí mnoho možností: 3D rekonstrukce, rekonstrukce řezů v jiných rovinách než je rovina axiální. Novinkou jsou pak vícevrstvové CT tzv. multi-slice CT (Toshiba, Aquillion, 1999), které jsou vybaveny několika kruhovými systémy detektorů a umožňují tak získávání více řezů v několika sousedních rovinách v jednom okamžiku, a tak dále urychlují celý proces, a kladou tak menší nároky na pacienta.
- generace: Zdrojem záření je zde elektronové dělo. Zařízení typu Imatron se liší tím, že masivní anoda je orientovaná jako výseč kolem části obvodu nemocného a má několik prstenčitých ohnisek. Nehýbe se zde žádná složka. Zařízení se budí současně na několika ohniscích a dopadá na dva prstence detektorů – získání několika vrstvových záznamů současně, za extrémně krátké expozice 50ms.
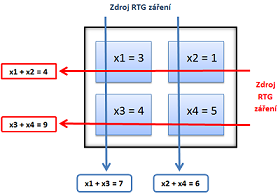
Princip počítačové tomografie
Při samotném vyšetření je pacient fixován na posuvném lůžku, které postupně prochází snímacím stojanem. Na jedné straně stojanu je štěrbinový zdroj rentgenového záření (rentgenka) a na opačné straně scintilační detektory. U starších tomografů jsou detektory umístěny proti rentgence, pohybují se spolu s ní a jsou s ní pevně spojeny. U modernějších tomografů jsou nepohyblivé detektory prstenčitě uspořádány kolem celého pacientova těla. Nejmodernější technikou je spirální CT, kde rotuje jak vyšetřovací stůl, tak tunel přístroje. Pacient je osvěcován postupně bod po bodu a výsledkem je transverzální řez těla. Výsledný řez je tedy počítačovou rekonstrukcí mnoha,,klasických´´ RTG snímků určité roviny. Záření je zachycováno pomocí systému detektorů připojených k počítači.
Rentgenka pracuje pulzně (1 pulz trvá 1–4 ms). Rentgenový paprsek má vějířovitý tvar. Rentgenové záření následně vniká do pacientova těla a částečně se absorbuje. Scintilační detektory zaznamenají míru (koeficient) zeslabení záření μ a údaje převedou do paměti počítače. Potom se systém rentgenka-detektor pootočí o určitý úhel a děj se opakuje. Na konci vyšetření počítač zpracuje údaje a zobrazí tomogram, který je dán hodnotami absorpčních koeficientů μ z jednotlivých míst daného řezu. Zjišťujeme tedy hodnotu absorpce rentgenového záření v malých objemových částečkách, které nazýváme voxely (volume matrix element) – je to vlastně analogie pixelu v planárním obraze, ale každý voxel nepředstavuje dvourozměrnou jednotku, ale má také svou hloubku danou tloušťkou řezu. Výsledkem je rekonstrukce příčné vrstvy tělem nemocného=AXIÁLNÍ VRSTVA, zatím co u klasické tomografie se podle polohy nemocného získávají VRSTVY FRONTÁLNÍ nebo SAGITÁLNÍ.
Hounsfieldovy jednotky, vznik obrazu
Transversální řez zobrazovaného objektu počítačovou tomografií je tvořen více než 250 000 voxely, tj. malými jednotkami objemu tkáně s různou průměrnou absorpcí a rozptylem použitého RTG záření. Ke zjištění absorpce voxelu je třeba, aby jím záření prošlo opakovaně a to pod různými úhly. Výsledná hodnota absorpce voxelu (tj. míra absorpce a rozptylu procházejícího záření) je následně vyjádřena pomocí denzitní jednotky – Hounsfieldovy jednotky [HU] (CT číslo), která vyjadřuje absorpci záření daného voxelu vztaženou k absorpci záření vody (pro vodu platí HU = 0). Detektory následně zjišťují součet absorpcí všech voxelů, kterými paprsek prošel.
Hounsfieldovy jednotky [HU] (CT čísla) jsou tedy vyjádřením denzity (míry absorpce a rozptylu záření) konkrétních voxelů. Pro každý voxel je z naměřené hodnoty absorpce vypočítána příslušná HU, která je vztažena k hodnotě absorpce RTG záření vodou.
Hodnota HU je definována podle vztahu:
kde k – smluvená konstanta o velikosti 1000
kde μ – koeficient zeslabení vyšetřované tkáně
kde μw – koeficient zeslabení vody (adsorpční koeficient μw = 0,22 cm−1)
V praxi mohou nabývat Hounsfieldovy jednotky hodnot od −1000 (vzduch), do cca 1000 (kompaktní kost). Pro diagnostické užití a pro zobrazení výsledného obrazu v odstínech šedi na monitoru (viz dále) je tedy k dispozici cca 2000 čísel.
Počítač využívá k zjišťování absorpčních hodnot, nezbytných pro výpočet Hounsfieldových jednotek, Fourierovu transformaci. Konkrétní řez je pořízen velmi rychle (5–7 s), což usnadňuje zobrazení některých orgánů (například střev, kde peristaltika vede k rozostření obrazu) a umožnilo vyšetření srdce a velkých tepen. Obraz vzniká na monitoru již během řezu, dokončen je však až po skončení celého snímání. Počítač musí dále provést řadu korekcí, například odstranit artefakty, které vznikají na rozhraní kosti a měkké tkáně (tzv. Hounsfieldův efekt), které je způsobeno tím, že kost absorbuje více měkčí záření než tvrdší.
Po naměření hodnot absorpcí jednotlivých voxelů a výpočtu příslušných Hounsfieldových jednotek, jsou tyto hodnoty převedeny na monitor, kde konkrétním hodnotám Hounsfieldových jednotek odpovídají konkrétní odstíny šedi. Tak vzniká výsledný CT obraz vyšetřovaného orgánu.
Počítač tedy převádí analogový signál na digitální, který dále zpracovává a nakonec jej opět převádí na analogový (výsledný obraz). Stejně jako RTG je i CT zobrazením denzit. Naměřená data (jednotlivé snímky) jsou následně složitými matematickými postupy rekonstruovány do výsledné matice.
| Tkáň | CT číslo, densita HU |
|---|---|
| vzduch | −1000 |
| tuk | −50 – −100 |
| voda | 0 |
| likvor | 5 |
| bílá hmota mozková | 30 |
| šedá hmota mozková | 34 |
| krev | 47 |
| játra | 40–60 |
| svaly | 35–75 |
| vazivové tkáně | 60–90 |
| chrupavka | 80–130 |
| kost | 1000–3000 |
Zpracování CT obrazu
Jak bylo uvedeno výše, pro zobrazení výsledného CT snímku na monitoru lze využít cca 2000 hodnot HU, které mohou být teoreticky převedeny na odpovídající počet odstínu šedé. Lidské oko však dovede rozlišit maximálně okolo 25 odstínů. Při zobrazení CT snímku není proto celý rozsah Hounsfieldových jednotek zdaleka využíván.
V praxi leží většina hodnot měkkých tkání v rozsahu HU 0–100. Při praktickém použití se tak odstíny šedi pro zobrazení na monitoru přiřazují jen v tzv. absorpčním oknu hodnot – tj. v rozsahu, ve kterém leží hodnoty HU, které jsou pro zobrazovaný orgán směrodatné a vypovídající (standardně právě rozsah cca HU 0–100). Díky adsorpčnímu oknu hodnot se zobrazí detailně pouze požadovaný obraz a zároveň je bezpečně "srozumitelný pro lidské oko, protože využívá takové množství odstínu šedé, které oko bezpečně rozliší.
Výhody CT zobrazení
- Umožňuje zobrazit i málo kontrastní měkkou tkáň včetně nádorů a to díky:
- vysoké citlivosti scintilačních detektorů,
- velmi rychlému zpracování údajů ze scintilačních detektoru.
- Metoda výhodná i pro plánování chirurgických zákroků a radioterapie zhoubných onemocnění,
- velmi dobrá rozlišovací schopnost a kontrast → obraz je ostřejší,
- eliminace odrazů a jejich interferencí,
- výsledky se dají uchovat v počítači, část obrazu se dá zvětšit a detailně zkoumat,
- radiační zátěž pacienta při CT můžeme srovnat s dávkou záření při klasickém vyšetření.
Nevýhody CT zobrazení
- Vysoká pořizovací cena zařízení,
- jejich obsluha vyžaduje přítomnost vysoce školeného personálu.
Součásti CT
- Vyšetřovací stůl s úložnou deskou pro pacienta – deska je posuvná a její posun lze řídit počítačem,
- portál (gantry) – vyšetřovací tunel, kterým projíždí deska, na které je uložen pacient; jedná se o skříň obsahující rentgenku, detektory a mechanismus, po němž se rentgenka a případně i detektory pohybují, a další zařízení, včetně chladícího systému,
- – uprostřed je kruhový otvor pro vyšetřovací stůl, který je pohyblivý vertikálně, podélně i do strany, takže dovoluje zasunout nemocného do různé hloubky gantry,
- – musí mít postačující průměr (až 84cm), aby v něm mohli pohodlně ležet i obézní pacienti a udržovat stálou polohu což je pro vyšetření zásadní požadavek, protože jakákoliv změna polohy nemocného zkreslí výsledek jak dané vrstvy, tak i možnost srovnání vrstev mezi sebou,
- – gantry je možno omezeně (do 30°) naklánět a volit tak rovinu řezu (např. ortográdní projekce),
- vysoce výkonná rentgenka,
- detektory – jsou kalibrovány tak, aby odpověď všech detektorů na náraz fotonu rentgenového záření byla stejnoměrná,
- – po nárazu fotonu se musí co nejrychleji vrátit k nulové hodnotě,
- vysoce výkonný rentgenový generátor,
- – rentgenky musí být v CT výkonné a tepelně odolné protože jejich zátěž je mimořádně velká, pulzní obsluha a dokonalé chlazení jsou nezbytné pro dobrou funkci,
- stůl operátora – obsahuje klávesnici a obrazový a textový monitor,
- počítače – řídící počítač (ovládá a řídí akvizici snímků) a vyhodnocovací počítač (ze surových dat - tzv. raw data - rekonstruuje obrazy a dále je zpracovává),
- diagnostický stůl – určen ke studiu obrazů lékařem,
- dokumentace – například na optické nebo magnetické disky, diskety nebo záznam na filmovém materiálu.
Detektory
CT zařízení se liší velikostí, typem, počtem a uložením detektorů. Větší účinnost detektorů vede k lepšímu rozlišení kontrastů a větší počet detektorů k lepšímu prostorovému rozlišení.
Typy detektorů:
- scintilační,
- proporcionální (plynové),
- keramické.
1. Scintilační krystaly
- NaI(Tl) – scintilace v UV spektru, prostorově náročný
- CsI(Tl) – scintilace ve viditelném spektru, prostorově úsporné
- dlouhá "mrtvá doba", je třeba vysoce stabilní zdroj vysokého napětí, náročné sjednotit vlastnosti jednotlivých detektorů.
2. Proporcionální detektory
- méně závislé na stabilizovaném vysokém napětí, jednoduchá konstrukce, uniformní vlastnosti, tepelně stabilní
- prostorově náročný,nízká rozlišovací schopnost, malá účinnost.
3. Keramické detektory
- sycené prvky vzácných zemin – YGdEu2+O3 (ytrium-gadolinium oxid),
- scintilace ve viditelném spektru,
- vysoká absorpční schopnost, vhodné mechanické vlastnosti,
- ekonomicky nedostupné pro běžné aplikace.
Angiografie
Angiografie znamená vyšetření cév zobrazovací metodou. Samotný termín v užším slova smyslu značí klasickou angiografii, kdy se skiagraficky zobrazí tepna po naplnění kontrastní látkou. Zobrazení je nutno provádět minimálně ve dvou projekcích jako u RTG kostí, poněvadž stenóza může být asymetrická a v jedné projekci se tak nemusí zobrazit.
Kromě morfologické diagnostiky lze provádět selektivní odběry krevních vzorků z cév (např. u endokrinně aktivních tumorů pankreatu či nadledvin), selektivní zavádění katetrů např. pro lokální chemoterapii (např. do a. hepatica propria) a další.
- Arteriografie: zobrazení tepen.
- Flebografie: zobrazení žil.
- Kavografie: zobrazení duté žíly.
- Portografie: zobrazení portálního žilního systému.
Procedura a kontrastní látky
Nejčastěji se katetr zavádí do femorální tepny tak, aby se vyšetřující dostali do levé komory. Po celý průběh vyšetření je vše sledováno na monitoru. Nejčastěji pomocí Digitální subtrakční angiografie – DSA o 2–3 obr/sec. Nepoužívá se však u srdce, to je potřeba sledovat 15–30 obr/sec. Je důležité si uvědomit, že čím více obrázků, tím více záření do těla proniká.
Kontrastní látky využívané v angiografii
Jodové kontrastní látky
- Základem je benzenové jádro s připojenými 3 atomy jódu.
- Vylučovány ledvinami.
- Ionické (disociace na elektricky nabité ionty) a neoinické (bez disociace, lepší snášenlivost).
Gadoliniové kontrastní látky
- Určené pro MR, MRA.
- Výrazně nižší alergenicita.
Alternativní KL: Oxid uhličitý
- Určené především pro pacienty s rizikem vzniku alergické reakce a dále u lidí s poruchou funkce ledvin.
- Vyšetření břišní aorty a tepen dolních končetin.
- Obtížná aplikace.
Digitální subtrakční angiografie – DSA
Klasická invazivní metoda angiografického vyšetření, kdy je možné provést zároveň i angioplastický zákrok, jako je například rozšiřování zúžených cév pomocí implantace stentu.
Postup
U DSA se odečítá maska nativního obrazu. To znamená, že samotné snímání probíhá ve dvou fázích, abychom ze snímku mohli odstranit obraz „stínící“ tkáně, přes kterou by bylo nemožné vidět obraz zkoumané cévy, cévního řečiště (kostní tkáň, apod.).
Využívámé subtrakce, tedy odečtení obrazů:
- První snímání probíhá bez použití jakékoliv látky a následuje převedení obrazu do negativu.
- Dále je přímo do tepny vpravena kontrastní látka (jde tedy o tzv. intraarteriální DSA) a následuje druhé RTG snímání. Poté lze pomocí počítačové techniky oba obrazy odečíst (subtrakce) a vzniká přesný obraz dané cévy. Kontrastní látka je nejčastěji jodového charakteru.
Nejčastějším přístupovým místem je arteria femoralis communis.
| DSA: stenóza společné ilické tepny, stent |
| DSA: stenóza dialyzačního shuntu, PTA |
| DSA: embolizace krvácení do tlustého střeva |
Selektivní koronarografie – SKG
SKG je angiografické vyšetření koronárních tepen při jejich selektivním nástřiku kontrastní látkou na bázi jodu. Lokálně se umrtví kůže a zavede se katetr do femorální nebo radialní tepny. Jakmile je katetr na místě, je možné provádět celou řadu procedur: angioplastiku, odstraňování hematomu, elektrofyziologické studie nebo pouštění další kontrastní látky.
CT angiografie
Neinvazivní metoda angiografického vyšetření krevního řečiště. V tomto případě je nejčastějším přístupovým místem periferní žíla, tedy často loketní jamka.
Rozlišujeme CT angiografii tepen a CT flebografii (tedy angiografii žil).
CT angiografie tepen (angio-CT / CTA)
CT vyšetření v arteriální fázi, kdy má tepna nejlepší náplň kontrastní látkou. Ke správnému načasování spuštění skenu se používají různé metody:
(V praxi se často využívá modifikace, kdy se sleduje změna denzity lumen artérie vizuálně a v případě dostatečného vzestupu se skenování spouští ručně).
- Bolus timing – po podání malého bolusu kontrastní látky se stanovuje křivka denzit z lumen arterie v čase, ze které se pak odvodí nejvhodnější čas k zahájení skenování.
- Odhadem – nejrychlejší, s největším rizikem neoptimálního načasování.
CT flebografie – kavografie, portografie
CT vyšetření v portální fázi (portografie), pozdní žilní fázi (žíly), žilní předfázi (periferní žíly).
| CT břicha: trombóza portální žíly |
|
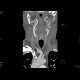
Angio-CT karotid: stenóza vnitřní karotidy |

|
CTA mozkových tepen: aneurysma |
MR angiografie – MRA
Neivazivní metoda angiografického vyšetření. Výhodou je absence ionizujícího záření.
MRA se používá pro vyšetření možných problému jako stenóza (zúžení průtoku krve), blokáda nebo aneurysma (zeslabení cévní stěny a riziko prasknutí). Často se používá na zobrazení krku, mozku a dalších.
Zobrazení
- Nativně metodou time-of-flight (TOF) či fázového kontrastu bez aplikace kontrastní látky.
- Nebo jako postkontrastní vyšetření po aplikaci kontrastní látky (kontrastní MRA) − využíváme paramagnetické cheláty gadolinia, který zesiluje kontrast, a tak dosahujeme zřetelnějších zobrazení.
V současnosti je kontrastní MRA velmi vhodnou miniinvazivní metodou pro detekci patologických stavů hrudní aorty, břišní aorty a jejích větví (arteriitida, disekce, okluze), i anomálií malého oběhu (arteriovenózní zkraty, anomální žilní návrat apod.). Vynikajících výsledků dosahuje kontrastní MRA v zobrazování magistrálních krčních tepen a renálních tepen. [4]
Je možné také 3D zobrazení tkání např. pomocí maximum intensity projection (MIP), kde se výsledky z laterální a axialní roviny spojí. Rozdíl od CT angiografie je, že nezobrazuje lumen.
Výhody
- Minimální nefrotoxicita a alergenicita v porovnání s jodovými kontrastními látkami
- Možnost využití u pacientů s diabetem, u kterých je přítomná silná kalcifikace stěn tepen a také nefropatie, což může být zhoršeno právě podáním jodové kontrastní látky, jak je tomu v přípdě DSA nebo CT angiografie
Komplikace
Způsobené zákrokem
Nejčastěji se u pacientů objevuje krvácení z místa vpichu do podkoží – hematom, kdy v případě, že je menší dochází ke spontannímu vstřebání. Větší krvácení se objevují méně často a to nesprávným vyjmutím zavaděče nebo v důsledku nedodržení doporučených nařízení, především klidu na lůžku.
Další komplikace se vyskytují velmi vzácně. Jsou popsány případy arytmie, uvolnění trombu nebo embolie vedoucí k mrtvici, krvácení. Vzácně dále dochází k poškození nervů, které se projevuje brněním.
Způsobené působením kontrastní látky
Nežádoucí reakce způsobené kontrastní látkou patří mezi tzv. systémové komplikace.
V praxi jej můžeme rozdělit následovně:
JODOVÉ KONTRASTNÍ LÁTKY
- Alergoidní: mírný až vysoký stupeň (křeče, hypotenze, tachykardie), nezávislý na množství podané KL, uvolnění histaminu a serotoninu
- Chemotoxické: úměrná reakce množství podané KL, vzniká po ovlivnění určitého orgánu → nefrotoxicita, kardiotoxicita, neurotoxicita
Ostatní KL používané v angiografii (gadoliniové, oxid uhličitý) nemají zásadní rizika ve spuštění nežádoucí reakce organismu.
RTG terapie
Rentgenové záření předává při průchodu hmotou svoji energii hmotě – způsobuje ionizaci atomů a molekul. V biologickém prostředí toto zvýšení energie zahájí sled pochodů vedoucí, dle množství absorbované dávky záření, k degenerativním pochodům na různých úrovních organismu. Tyto vlastnosti ionizujícího záření jsou využívány k léčení onkologických pacientů.
Rozdělení
Podle lokalizace, objemu a podle radiosenzitivity nádoru je volena pronikavost použitého záření.
- Povrchová radioterapie – užívá se na nádory na kůži, sliznicích, pracuje s napětím 50–60 kV
- Polohloubková radioterapie – terapie nádorů těsně pod kůží, používají se všechny konvenční rentgenové přístroje s nastavením energie fotonů do 100 keV
- Konvenční hloubková radioterapie – ozařování i hlouběji uložených nádorů, rentgenové přístroje s energií fotonů 200–400 keV
- Vysokovoltážní radioterapie – ozařování tumorů uložených v hloubce, energie okolo 1 MeV
Fyzikální pohled
Zdroje záření
- emitující gama záření
- Kobaltové radionuklidy (60Co) se používají pro hloubkovou radioterapii. Využívají se v Leksellově gama noži.
- Cesiové radionuklidy (137Cs) ozařují maximálně do hloubky 5 cm.
- terapeutické radionuklidy: radionuklidy, které se vpraví do těla a specificky se vychytávají v určitých tkáních
- 131I
- 85Sr
Urychlovače částic
- Kruhové: cyklotron, betatron (využití v BNCT, protonové terapii)
- Lineární urychlovač
- Buď se využívají přímo urychlené částice, nebo se nechají dopadnout na wolframový terčík, kde se zabrzdí, čímž vznikne vysokoenergetické rentgenové záření.
Medicínský pohled
Radioterapie se obecně dělí dle polohy zdroje záření na zevní (externí) radioterapii (teleterapie,TRT, ERT) a brachyradioterapii (brachyterapie, BRT).[5] U zevní radioterapie je zdroj záření mimo tělo ozařovaného pacienta, zpravidla ve vzdálenosti 80–100 cm od těla pacienta, resp. od osy rotace ozařovacího přístroje. Při brachyterapii je zdroj záření zaveden do těsné blízkosti ložiska nebo přímo do orgánu či tkáně s nádorem, event. do jeho lůžka. Obě metody se používají samostatně nebo se v indikovaných případech vzájemně kombinují.
Princip léčby ionizujícím zářením
Při radioterapii je cílem dostat maximum energie ionizujícího záření do oblasti nádoru a současně nepoškodit okolní zdravou tkáň. Při použití RTG záření je zářením zasažena tkáň před i za nádorem. Možnou dávku záření tedy určuje odolnost okolní zdravé tkáně. Intenzitu biologického účinku ozáření ovlivňuje:
- celková doba expozice, ale také časové rozdělení jednotlivých dávek v průběhu terapie
- prostorové rozložení ozáření - účinek se u stejných expozic zvyšuje s objemem ozářené tkáně
- kvalita záření - určuje se tzv. polotloušťkou - udává tloušťku určitého kovu, který sníží intenzitu záření na polovinu (v mm)
Léčba ionizujícím zářením je kvůli možným negativním biologickým účinkům využívána prakticky jen u onkologických pacientů.
Mechanismus biologického účinku ionizujícího záření
Průchod rentgenového záření biologickým prostředím způsobuje ionizaci a excitaci atomů a molekul buněk organismu, čímž vznikají chemicky vysoce aktivní látky. Rentgenové záření způsobuje nepřímou ionizaci. Na rozdíl od přímého účinku ionizujícího záření, kdy dochází k absorpci energie záření přímo v jádře, spočívá nepřímá ionizace v radiolýze vody se vznikem volných radikálů (H• a OH•). Radikály dále reagují s molekulami DNA, způsobují zlomy a jsou tedy příčinou poškození. Kromě radikálů vznikají ještě molekulární produkty radiolýzy (H2, O2, H2O2) s životností jen okolo 10-6 s, protože se rychle přeměňují na reakční produkty.
V řetězci reakcí následujícím po radiolýze je velice důležitá přítomnost kyslíku, ovlivňuje totiž radiosenzitivitu buněk. Tkáně s menším obsahem kyslíku mohou být více odolné. Přítomnost kyslíku zvyšuje vznik radikálů a brání reparativním pochodům v buňce. Buňky s dostatečným zásobením kyslíkem jsou 2–3x citlivější na záření.
Protonová terapie
Protonová terapie je druh radioterapie vyvíjený pro léčbu onkologických onemocnění. Hlavní výhodou protonové terapie by mělo být lepší zacílení předávané energie na nádor, menší poškození okolní tkáně a tím i menší vedlejší účinky než u běžné (fotonové) radioterapie. Korpuskulární charakter protonů na rozdíl od fotonů způsobuje, že protony předávají tkáním před nádorem relativně málo energie a po předání maxima své energie na zaměřené místo (Braggův vrchol) se prakticky zastavují. To by mělo dovolovat použití větší dávky záření a zvýšit pravděpodobnost likvidace nádoru. Uvedené výhody by měly být největší při ozařování nádorů v blízkosti citlivých struktur (nádory mozku, krku, očí, slinivky břišní, jater, nebo prostaty). Do jaké míry protonová terapie skutečně naplní uvedená očekávání, je stále předmětem výzkumu; dosavadní výsledky jsou kontroverzní[6].
Výroba protonů vyžaduje cyklotron či synchrotron a další velmi nákladná zařízení. Jelikož je Braggův vrchol široký jen několik milimetrů, je potřeba protony rozptýlit, aby pokryly celé ložisko. Toho se dociluje pomocí pomůcek (rozptylovací filtry, modulační kotouče, kompenzátory), které jsou rovněž velmi nákladné. První pokusy s protonovou terapií začaly v padesátých letech 20. století, rozsáhlejší výzkum se rozběhl až na přelomu 20. a 21. století.
Fyzikální podstata
Protonové záření je označení radiace způsobené proudem protonů, jedná se tedy o korpuskulární záření. Protony jsou kladně nabité částice, jejichž náboj je roven +1 e, a mají nenulovou klidovou hmotnost. Díky těmto jejich fyzikálním vlastnostem je protonový svazek v určitých případech léčby výhodnější než konvenční radioterapie fotony. Zdrojem protonů je vodík, zdrojem protonového svazku pak urychlovač částic. Svazek nemá téměř žádný boční rozptyl a je možné ho velmi přesně zacílit a přizpůsobit tvaru nádoru. Pronikavost svazku se pohybuje mezi zářením α a β. Při vstupu do tkáně a dalším průchodu předávají urychlené protony jen malé množství své energie, zhruba 30 %. Jadernými reakcemi a srážkami s jádry a atomovými elektrony protony ztrácí rychlost a jejich ionizační účinky sílí. Maximální radiační dávku předají tkáni těsně před koncem doletu v oblasti tzv. Braggova vrcholu (Bragg peak), tkáň zde absorbuje přibližně 70 % energie svazku. Dosah svazku, tedy hloubka Braggova vrcholu, je přesně určen vstupní energií protonů, kterou lze regulovat, právě v závislosti na hloubce nádorového ložiska (až 30 cm). Po vydání veškeré energie se částice zastaví a dál v letu nepokračují, tím pádem nejsou tkáně za nádorem ozařováním poškozeny.
Svazkem protonů chápeme soubor nabitých částic pohybujících se po blízkých dráhách, který má ohraničené příčné rozměry. Pro jeho přípravu se v protonové terapii využívají urychlovač – cyklotron, případně jeho varianta synchrocyklotron. Jejich úlohou je zvýšit kinetickou energii nabitých částic na požadovanou úroveň a sjednotit jejich dráhy, aby vznikl jednotný paprsek. Jde o kruhové (cyklické) urychlovače. V porovnání s lineárním urychlovačem je možné využít menšího urychlovacího napětí. Princip urychlení částic v cyklotronu spočívá v oběhu částic po kruhových dráhách – částice tak získá mnohem větší energii, než by jí byla přidělena při jediném lineárním přeletu trubicí. Energie protonů se pohybuje v rozmezí 70 – 230 MeV. V urychlovacích zařízeních je nastavitelná pro různé typy nádorů, například u nádoru oka postačuje energie protonů přibližně 70 MeV. V případě, že je urychlovač schopen udělit částici energii kolem 300 MeV, může být využit i k protonové tomografii
Proud protonů procházející tkání působí přímou ionizaci a excitaci molekul a atomů tkáně. Touto ionizací dochází k poškození molekul DNA a to buď přímo nebo nepřímo (ionizací dojde ke vzniku volných radikálů a ty mohou reagovat s molekulami DNA a způsobit poškození). Buňky mají reparační mechanizmy, které jsou schopny vzniklá poškození DNA opravit. U nádorových buněk jsou tyto mechanizmy narušeny a nádorové buňky pak nemají dostatečnou schopnost opravy DNA. To činí nádorové buňky citlivější vůči ozařování. Z toho lze usoudit, že cílem terapie je způsobit dostatečné poškození DNA nádorových buněk, aby tyto zanikly nebo se přestaly dělit. Tohoto efektu není nutně dosaženo jedním ozářením, ale poškození se mohou kvůli snížené reparační schopnosti nádorových buněk kumulovat.
Technické provedení
Protonový ozařovač je poměrně nákladné a složité zařízení. Jeho vývoj je úzce spjat s vývojem cyklotronů, které jsou nejběžnějším způsobem tvorby urychleného svazku protonů pro potřebu ozařování.
Většina dnešních moderních přístrojů se skládá ze tří základních částí:
- Cyklotron
- Systém transportu a energetické modulace částic
- Ozařovací tryska (nozzle)
Samotný protónový ozařovač doplňují technická řešení jednotlivých protonových center. Velmi důležitou roli hrají zejména:
Cyklotron
Cyklotron je cyklický vysokofrekvenční urychlovač nabitých částic (neurychluje např. neutrony, protože nemají náboj). Obsahuje dvě duté polokruhové elektrody – duanty, silný elektromagnet a zdroj vysokofrekvenčního napětí. Duanty jsou natočeny otvory proti sobě, mezi sebou však mají prostor. Do tohoto prostoru jsou vystřeleny částice (v našem případě protony), které jsou urychleny vysokofrekvenčním elektrickým polem (o napětí 10kV - 1000kV) do doby, než vstoupí do duantu. Duanty působí jako Faradayovy klece, takže v nich na částice nepůsobí elektrické pole. Působí na ně jen pole magnetické, které je orientováno kolmo na směr jejich pohybu. Magnetické pole zakřivuje pohyb částic - zapříčiňuje kruhové zakřivení. V dutinách duantů částice urychlovány nejsou, jsou pouze usměrňovány. Pohyb protonů je urychlen pouze v prostoru mezi duanty. Částice cyklicky procházejí systémem duant 1 – mezera mezi duanty – duant 2 – mezera atd. Postupem času nabírají rychlost a zvětšuje se poloměr dráhy. Při dosažení maximální rychlosti se částice dostávají k okraji cyklotronu, odkud jsou speciálními vychylovacími magnety usměrněny do transportního systému protonového ozařovače. Svazek protonů může při maximální rychlosti (přibližně 60% rychlosti světla) dosáhnout kinetickou energii až 230 MeV. Rychlost i energie svazku částic jsou před vstupem do transportního systému konstantní.
Systém transportu a energetické modulace částic
K transportu protonů dochází ve vakuové trubici, ve které je paprsek protonů (za pomoci elektromagnetů) zaostřován a ohýbán směrem do terapeutické místnosti. Jelikož v cyklotronu vznikají i částice o jiné než požadované energii je zapotřebí modulace svazku, ke které u novějších přístrojů dochází precizním upravením magnetického pole cívek na cestě vakuovou trubicí a u starších typů se používá rotačních modulátorů (mechanické oddělení) zamezujících postupu protonům s jinou než danou rychlostí.[1] [2]
Ozařovací tryska
Ozařovací tryska (nozzle) je velmi složité zařízení, které stojí až na samém konci procesu vyzáření protonového svazku. Jelikož nádory, které jsou objektem léčby protonovým ozařovačem, mají určitý objem a zpravidla nepravidelný tvar, i princip vyzařování protonů se musel modifikovat. Ke komplexnímu pokrytí tumoru je svazek potřeba rozšířit do dvou směrů – laterálně a distálně, přičemž ozařování se provádí z více úhlů. Protonová centra jsou vybavena univerzálními tryskami, které musí obsahovat fixní rozptylový filtr a sekundární rozptylový filtr, které se starají o rozptýlení svazků. Chybět nesmí ani modulační kotouč, který má na starost rozdělení svazků do určitých energických intervalů, aby došlo k zasažení nádoru v celé jeho hloubce. Další části, které slouží ke korektnímu vyzáření, jsou skenovací magnety, kompenzátor a clona. Momentálně existují dva typy těchto zařízení, a to trysky pracující na principu pasivního rozptylu svazku a trysky založené na principu aktivního skenování.
Ozařovny
Trysky se nacházejí v místnostech – ozařovnách. Najčastěji se vyskytují dva typy ozařoven – se svazkem pevným (Fixed beam treatment rooms) a se svazkem pohyblivým (Gantry treatment rooms)[3]. V ozařovně s pohyblivým svazkem je nádor ozařován pohyblivými tryskami z několika úhlů. Svazky protonů se protínají v izocentrickém bodě, orientovaném v místě nádoru. Ozařovny s pevným svazkem mají trysku pevně ukotvenou, modulovaná je pouze poloha pacienta. Speciálním typem ozařovny je například ozařovna na oční nádory. Pacient má hlavu upevněnou v křesle a pohyby trysky jsou synchronizovány s jemnými pohyby oční bulvy.
Indikace
Využití protonové terapie se zkouší především u nádorů, které se nacházejí v blízkosti citlivých struktur. Za nejvhodnější se zatím protonová terapie považuje u mnohých nádorů dětského věku, dle některých recentních studií však nepřináší terapeutické výhody proti standardním přístupům[7]. Dále bývá protonová terapie doporučována při léčbě očních melanomů, chondromů a chondrosarkomů. Pro mnoho dalších typů nádorů byly publikovány slibné výsledky, vycházejí však ze studií s malými počty pacientů[6]. Z nádorů ORL je protonová terapie vhodná u karcinomu nosohltanu, kde chirurgický přístup prakticky není možný.
Srovnání s konvenčním ozařováním
Protonové ozařování a konvenční radioterapie se liší v efektivitě zacílení na dané místo v těle člověka. Obecně platí, že ke zničení buněk je potřeba co největší dávka ozáření v co nejkratším čase. Maximální dávka ozáření, která může být použita v konkrétním případě, se odvíjí od možnosti poškození okolní zdravé tkáně.
Konvenční radioterapie předává největší dávku záření už při vstupu do tkáně. V cílené oblasti je pak dávka střední a dál je předávána menší dávka. Dalo by se říci, že dávka plynule klesá směrem od zdroje. Ozáření zdravých tkání má za následek vedlejší účinky léčby. Ty mají vliv na celkový stav těla, kvalitu života a s tím i rychlost uzdravení.
Při protonové terapii se při vstupu do tkáně předá asi 20–30 % energie, do cílené oblasti 70–80 % energie. Cílení je možné s milimetrovou přesností. Tkáň za cílenou oblastí je ozářena velmi málo. Konstrukce ozařovačů a plánování terapie umožňuje ozařovat i složitě tvarované oblasti s vysokou přesností.
Na základě výše zmíněného lze předpokládat, že při protonové terapii je možno do cílené oblasti dodat několikanásobně vyšší energii, než je možné při použití konvenčních metod ozařování. Radiační zátěž okolních tkání je při tom relativně nízká. To by mělo být výhodné zvlášť v případech, kdy je cílená oblast v blízkosti tkání velmi citlivých na ozáření (sliznice zažívacího a močového traktu, lymfatická tkáň, kostní dřeň, pohlavní žlázy, tkáně vyvíjejícího se organismu dětí). Pro potvrzení tohoto předpokladu však prozatím chybí dostatečně silná data[8] a někteří autoři upozorňují, že vzhledem k různé povaze záření nelze při odhadování účinků protonového záření nekriticky vycházet ze zkušeností s fotonickou léčbou[6]
Přednosti protonové léčby, video s popisem
Vývoj oboru
Protonová terapie je v současné době považována za novinku v léčbě nádorových onemocnění, nicméně myšlenku, používat protony k léčebnému využití, vyslovil americký fyzik Robert R. Wilson, Ph.D již v roce 1946, kdy se podílel na výstavbě Harvardského cyklotronu (The Harvard Cyclotron Laboratory).
V roce 1948 Berkely Radiation Laboratory provedla obsáhlou studii o protonech, a potvrdila domněnky R. Wilsona. O několik let později – v roce 1954 zde byly protony poprvé použity k léčbě pacientů. V této laboratoři dosahovaly protony kinetické energie 100 MeV. Úspěchy se v roce 1958 podařilo zopakovat i u pacientů ve Švédsku v Uppsale – protony zde mohly dosáhnout kinetické energie 185MeV, Harvardský cyklotron ošetřil prvního pacienta až v roce 1961. Tento cyklotron byl sice uveden do provozu v roce 1949 a měl být schopen urychlit protony natolik, že jejich kinetická energie měla dosahovat až 160MeV, nicméně kvůli technickým potížím často dosáhla jen 95 – 110 MeV. Plné funkčnosti dosáhl cyklotron až o 6 let později.
Léčba ve fyzikálních laboratořích ale byla limitována jen na několik míst na těle, protože urychlovače nebyly primárně stavěny k léčbě pacientů. Částice neměly dost vysokou energii na to, aby dokázaly léčit i nádory, které se nacházely hlouběji v těle. Během sedmdesátých letech se tedy výzkum zaměřil na vývoj dokonalejších cyklotronů, výrazně tomu pomohlo sestavení dokonalejších počítačů koncem sedmdesátých let. Velká část technologií, které se dnes považují za standardní součást protonové terapie, vznikly mezi lety 1970 – 1990.
V roce 1990 byl v Loma Linda University, Kalifornie, otevřen první urychlovač, který se nacházel přímo v nemocnici, čímž bylo zajištěno zkvalitnění péče o pacienty.
Rozdíly v tom, jaké nádory centrum léčí, jsou tedy hlavně způsobeny tím, jak moc je daný cyklotron schopen protony urychlit (zvýšit jejich kinetickou energii). Protony s menší kinetickou energií nejsou schopny pronikat tak hluboko do tkání, proto se mohou používat jen k terapii nádorů, které se nacházejí blíže k povrchu těla (například nádory očí).
Evropa
Jedno z prvních center postavených v Evropě byl Paul Scherrer institut ve Švýcarsku, otevřený v roce 1984, nicméně se specializoval pouze na nádory očí. V roce 1991 bylo otevřeno Centre de protonthérapie de l‘Institute Curie v Orsay, které léčí pacienty s různými druhy nádorů. Po roce 2000 se dramaticky zvýšil počet protonových center, souvisí to s nárůstem počtu soukromých firem, které se zabývají vývojem nových cyklotronů. Do této doby byl výzkum financován především ze státních nebo univerzitních peněz.
| Centra v Evropě | Maximální dosažitelná kinetická energie (MeV) | Co léčí | Rok vzniku | Země | Web |
|---|---|---|---|---|---|
| The Clatterbridge Cancer Centre | 62 | Pouze nádory očí | 1989 | Velká Británie | https://www.clatterbridgecc.nhs.uk/ |
| Centre de protonthérapie de l'Institut Curie | 235 | Nádory očí, hlavy a některé nádory na páteři. U dětských pacientů také některé druhy nádorů hrudníku a břicha. | 1991 | Francie | https://curie.fr/liste/centre-de-protontherapie |
| Centre Antoine Lacassagne | 63 | Pouze nádory očí. | 1991 | Francie | http://www.centreantoinelacassagne.org/ |
| Paul Scherrer Institut | 250 | Nádory očí, hlavy a některé nádory na páteři. Některé nádory u dětí. | 1984 | Švýcarsko | https://www.psi.ch/protontherapy/ |
| Instytut Fizyki Jądrowej PAN | 60 | Nádory oční koule | 2009 | Polsko | https://www.ifj.edu.pl/ |
| Rinecker Proton Therapy Center | 250 | Nádory plic, jater, jícnu, hltanu, hlavy, očí, slinivky, prostaty, gynekologické nádory, nádory kostí | 2009 | Německo | https://www.rptc.de/de/ |
| ISL | 250 | Nádory očí | 1998 | Německo | https://www.helmholtz-berlin.de/zentrum/index_de.html |
| Westdeutsches Protonentherapiezentrum Essen | 230 | Nádory hlavy, páteře a oblasti pánve | 2013 | Německo | https://www.wpe-uk.de |
| Proton Therapy Centre Prague | 230 | Nádory ležící v oblasti páteře a v oblasti baze lební, nádory oka, prostaty, hlavy a krku, plic | 2012 | Česká republika | https://www.ptc.cz/ |
Činnost těchto a dalších center celosvětově koordinuje Particle Therapy Co-Operative Group, která doporučuje budovat jedno protonové centrum pro potřeby přibližně 10 mil. obyvatel. Seznam existujících, právě stavěných a plánovaných center lze dohledat na jejich stránkách.
Náklady
Protonová léčba využívá na rozdíl od tradičních forem ozařování proud protonů. I když využívá stejný princip výroby paprsků jako konvenční metoda, při protonové léčbě lze distribuci energie protonů nasměrovat. Proto je cena této terapie více než dvakrát vyšší než při fotonové metodě. Konkrétní hodnoty se ovšem odvíjí od regionu, přístrojů a příspěvků zdravotních pojišťoven. Cena za nákup všech vyžadovaných přístrojů se může vyšplhat velice vysoko. Například cena cyklotronu se pohybuje okolo 2 miliard korun českých.[9].
Hadronová terapie
Jedná se o ozařování nádorových struktur, při kterém se využívá těžkých nabitých částic, patřících mezi hadrony (protony – patřící mezi nejlehčí baryony a mezony π). Na rozdíl od lehkých částic (foton a elektron), které při srážce s jiným elektronem předávají velkou část své energie, nebo zcela změní svůj směr letu, těžké hadrony předávají při srážkách jen malou část své energie a jejich směr letu se mění jen minimálně. Hadrony tedy svou energii při průchodu tkání ztrácejí postupně, a proto se nerozptylují a všechny doletí zhruba do stejného místa. Čím rychleji částice letí, tím méně energie při cestě ztrácí. Směr letu částic lze korigovat pomocí magnetického pole, a tak se dá velmi přesně určit místo, dopadu hadronů. Nádor je pak velice přesně zničen bez větších zásahů do okolní tkáně.
Ozařování pomocí hadronů je známo již od roku 1954. Zatím ale stále nevyřešeným problémem zůstává urychlovač hadronů, který je nezbytnou avšak velice nákladnou součástí takového zařízení. Navíc je toto ozařování vhodné zhruba pro 5–10 % pacientů s rakovinou. Nádor se u nich nachází hluboko a je dobře lokalizován. Nejčastěji tedy nádory na mozku, u kterých obzvláště záleží na odstranění nádoru bez sebemenšího poškození okolní zdravé tkáně.
Nevýznamější modelitou hadronové terapie v Čechách je protonová terapie.
Reference
- ↑ a b c NAVRÁTIL, Leoš a Jozef ROSINA, et al. Medicínská biofyzika. 1. vydání. Praha : Grada, 2005. 524 s. s. 436. ISBN 80-247-1152-4.
- ↑ KUPKA, Karel, Jozef KUBINYI a Martin ŠÁMAL, et al. Nukleární medicína. 1. vydání. vydavatel, 2007. 185 s. s. 53. ISBN 978-80-903584-9-2.
- ↑ KUPKA, Karel, Jozef KUBINYI a Martin ŠÁMAL, et al. Nukleární medicína. 1. vydání. vydavatel, 2007. 185 s. ISBN 978-80-903584-9-2.
- ↑ DOC. MUDR. ŽIŽKA, PH.D, Jan. Současnost MR angiografie [online]. [cit. 2012-12-27]. <https://web.archive.org/web/20160331222721/http://zdravi.e15.cz/clanek/postgradualni-medicina/soucasnost-mr-angiografie-170739>.
- ↑ Radioterapie - učební texty pro studenty 5. roč. LF MU Brno. Klinika radiační onkologie, LF MU. Vypracovali: MUDr. L. Hynková, MUDr. H. Doleželová, Ph.D., prof. MUDr. P. Šlampa, CSc.
- ↑ a b c MOHAN, Radhe a David GROSSHANS. Proton therapy – Present and future. Advanced Drug Delivery Reviews. 2017, roč. ?, vol. 109, s. 26-44, ISSN 0169-409X. DOI: 10.1016/j.addr.2016.11.006.
- ↑ LEROY, Roos, Nadia BENAHMED a Frank HULSTAERT. Proton Therapy in Children: A Systematic Review of Clinical Effectiveness in 15 Pediatric Cancers. International Journal of Radiation Oncology*Biology*Physics. 2016, roč. 1, vol. 95, s. 267-278, ISSN 0360-3016. DOI: 10.1016/j.ijrobp.2015.10.025.
- ↑ TERASAWA, T., T. DVORAK a S. IP, et al. Systematic review: charged-particle radiation therapy for cancer. Ann Intern Med. [online]. 2009, vol. 151, no. 8, s. 556-65, dostupné také z <http://annals.org/aim/fullarticle/745053/systematic-review-charged-particle-radiation-therapy-cancer>. ISSN 1539-3704.
- ↑ LAYTON, Julia. Is proton therapy better than traditional radiation for cancer treatment? [online]. HowStuffWorks, [cit. 2017-01-05]. <https://health.howstuffworks.com/medicine/modern-technology/proton-therapy2.htm>.
Chybná citace: Nalezena značka <ref> pro skupinu „pozn.“, ale neexistuje příslušná značka <references group="pozn."/>